题目内容
17.下列说法正确的是( )| A. | 在海轮船壳上镶入锌块保护海轮,利用的是牺牲阳极的阴极保护法 | |
| B. | KNO3溶液和CH3OONH4溶液均显中性.两溶液中水的电离程度相等 | |
| C. | 若1 molNa2O2与足量水反应产生O2,理论上转移的电子数约为2×6.02×1023 | |
| D. | 用pH 均为2 的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 |
分析 A、原电池的正极金属易被保护,不易腐蚀;
B、酸或碱抑制水电离,含有弱根离子的盐促进水电离;
C、过氧化钠中氧元素的化合价为-1价,1mol过氧化钠与足量水反应生成0.5mol氧气,转移了1mol电子;
D、醋酸为弱酸,pH均为2的盐酸和醋酸溶液,两种溶液中H+离子浓度相等,则醋酸浓度大与盐酸,分别中和等物质的量的NaOH,当氢氧化钠恰好被完全中和时,消耗的两种酸的物质的量相等,根据n=C×V比较二者的体积关系.
解答 解:A、海轮外壳镶嵌锌块,此时铁作为原电池的正极金属而被保护,不易腐蚀,是采用了牺牲阳极的阴极保护法,故A正确;
B、KNO3溶液是强酸强碱盐,对水的电离无影响,CH3OONH4溶液是弱酸弱碱盐,促进水电离,故B错误;
C、1mol Na2O2与足量水反应生成0.5mol氧气,转移了1mol电子,转移的电子数为6.02×1023,故C错误;
D、醋酸为弱酸,pH均为2的盐酸和醋酸溶液,两种溶液中H+离子浓度相等,则醋酸浓度大与盐酸,设盐酸的浓度为C1,醋酸的浓度为C2,则C1<C2,分别中和中和等物质的量的NaOH,当氢氧化钠恰好被完全中和时,消耗的两种酸的物质的量相等,则有:n=C1V1=C2V2,因C1<C2,所以:V1>V2,消耗盐酸的体积更大,故D错误;
故选A.
点评 本题考查金属的腐蚀、水的电离、转移电子数的计算及弱电解质的电离,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力,有助于提升学生的学科素养,难度中等.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
8.在给定的条件下,下列物质间转化均能实现的是( )
| A. | Al2O3$→_{△}^{H_{2}}$Al$→_{常温}^{浓H_{2}SO_{4}}$Al2(SO4)3 | |
| B. | H2SiO3$\stackrel{△}{→}$SiO2$→_{△}^{盐酸}$SiCl4 | |
| C. | SO2$\stackrel{CaCl_{2}(aq)}{→}$CaSO3$\stackrel{O_{2}}{→}$CaSO4 | |
| D. | CH3CH3$→_{光照}^{Cl_{2}}$CH3CH2Cl$→_{△}^{NaOH醇溶液}$CH2=CH2 |
5.西维因是一种高效低毒杀虫剂,在一定条件下可发生水解反应:

有关说法正确的是( )

有关说法正确的是( )
| A. | 西维因分子式为C12H10NO2 | |
| B. | 西维因分子中至少有21个原子共平面 | |
| C. | 1mol西维因最多能与6mol氢气发生加成反应 | |
| D. | 取一段时间后的混合液,先用盐酸酸化,再滴加FeCl3溶液,可检验西维因是否发生水解 |
12.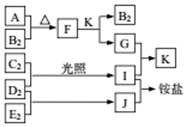 如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )
如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )
 如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )
如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下部是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态.下列说法正确的是( )| A. | B氢化物的沸点高于其同主族其它元素氢化物的沸点 | |
| B. | 原子半径大小:A>C>B>E>D | |
| C. | F中既含有离子键又含有极性共价键 | |
| D. | G中的阴离子能抑制水的电离 |
2.化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A. | 重大节日期间燃放的焰火的颜色是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 小苏打是制作馒头和面包等糕点的膨松剂,也是治疗胃酸过多的一种药剂 | |
| C. | 为防止月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| D. | 大力实施矿物燃料的脱硫脱硝技术,可以减少SO2、NO2的排放 |
9.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| B | 向滴有甲基橙的AgNO3溶液中滴加KCl溶液,溶液由红色变为黄色 | KCl溶液具有碱性 |
| C | 在CuSO4溶液中滴加KI溶液,再加入苯,振荡,有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为CuI |
| D | 某溶液滴加盐酸酸化的BaCl2溶液,生成白色沉淀 | 该溶液中可能不含SO42- |
| A. | A | B. | B | C. | C | D. | D |
6.下列图示与对应的叙述相符的是( )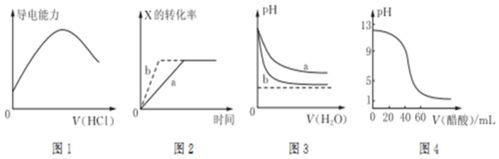

| A. | 图1表示向氨水中通入HC1气体,溶液的导电能力变化 | |
| B. | 图2所示反应:X(g)+2Y(g)?3Z(g),b曲线表示的一定是增大压强 | |
| C. | 图3可表示pH相同的NaOH溶液与氨水稀释过程的pH变化,其中曲线a对应氨水 | |
| D. | 图4可表示用0.100 0 mol/L,醋酸滴定40.00 mL 0.100 0 mol/L NaOH溶液得到的滴定曲线 |