题目内容
15. 铁与人类密切相关,几乎无处不在,地壳中大约5%是铁,是含量仅次于铝的金属.它的单质及化合物在科学研究和工业生产中具有许多用途.根据所学知识回答下列问题:
铁与人类密切相关,几乎无处不在,地壳中大约5%是铁,是含量仅次于铝的金属.它的单质及化合物在科学研究和工业生产中具有许多用途.根据所学知识回答下列问题:(1)基态铁原子的电子占据最高的能层的符号为N,与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素有5种.
(2)下列关于铁的说法,正确的是AB(填选项字母)
A.基态铁原子的电子排布式1s22s22p63s23p103d24s2肯定违反了泡利原理
B.铁属于黑色金属,在周期表中属于d区元素
C.铁丝可用于焰色反应实验时蘸取待测物,是由于铁在光谱图中无特征的谱线
D.Fe能与CO形成配合物Fe(CO)5,1mol Fe(CO)5中含有的σ键数是10NA
(3)某铁的化合物结构简式如图所示
①组成上述化合物各元素原子电负性由大到小的顺序为O>N>C>H>Fe
②上述化合物中氮原子的杂化方式为sp2、sp3
③在上图中用“→”标出亚铁离子的配位键.
(4)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N )和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是异硫氰酸
(5)铁单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如图A、B所示,若铁原子的半径是rcm,则这两种晶体密度之比是$\frac{3\sqrt{6}}{8}$.

分析 (1)Fe原子的电子排布式是1s22s22p63s23p63d64s2,与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素的3d轨道电子数为1、2、3、5、10;
(2)A.3p能级有3个轨道,最多容纳6个电子;
B.黑色金属包括铁、铬、锰,d区元素包括ⅢB~ⅦB、Ⅷ族元素;
C.铁的焰色反应焰色反应发出的光不影响其它金属火焰颜色;
D.Fe(CO)5分子含有5个配位键,而CO分子中含有1个σ键;
(3)①非金属性越强,元素的电负性越大;
②化合物中形成C=N双键的N原子形成2个σ键,含有1对孤电子对,而形成单键的N原子,形成2个σ键,含有2对孤电子对,杂化轨道数目分别为3、4;
③C=N双键的N原子有1对孤对电子与亚铁离子之间形成配位键,另外N原子带1个单位负电荷,与亚铁离子之间形成离子键;
(4)异硫氰酸中 H-N 键极性强,分子间存在氢键,而硫氰酸分子间只存在分子间作用力;
(5)根据均摊法计算晶胞中Fe原子数目,可以计算晶胞质量之比,图A体心立方密堆积,晶胞棱长长度为$\frac{4r}{\sqrt{3}}$cm,图B为面心立方密堆积,晶胞棱长长度为$\frac{\sqrt{2}}{2}$×4r=2$\sqrt{2}$r cm,结合ρ=$\frac{m}{V}$计算.
解答 解:(1)Fe原子的电子排布式是1s22s22p63s23p63d64s2,电子占据最高的能层的符号为N,与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素的3d轨道电子数为1、2、3、5、10,还有5种,
故答案为:N;5;
(2)A.3p能级有3个轨道,最多容纳6个电子,选项中排列违反了泡利原理,故A正确;
B.黑色金属包括铁、铬、锰,d区元素包括ⅢB~ⅦB、Ⅷ族元素,故B正确;
C.铁的焰色反应焰色反应发出的光不影响其它金属火焰颜色,故C错误
D.Fe(CO)5分子含有5个配位键,而CO分子中含有1个σ键,1molFe(CO)5中含有的σ键数是6NA,故D错误,
故选:AB;
(3)①非金属性越强,元素的电负性越大,则电负性O>N>C>H>Fe,故答案为:O>N>C>H>Fe;
②化合物中形成C=N双键的N原子形成2个σ键,含有1对孤电子对,而形成单键的N原子,形成2个σ键,含有2对孤电子对,杂化轨道数目分别为3、4,N原子采取sp2、sp3杂化,
故答案为:sp2、sp3;
③C=N双键的N原子有1对孤对电子与亚铁离子之间形成配位键,另外N原子带1个单位负电荷,与亚铁离子之间形成离子键,标出亚铁离子的配位键为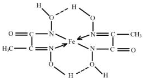 ,故答案为:
,故答案为: ;
;
(4)异硫氰酸中 H-N 键极性强,分子间存在氢键,而硫氰酸分子间只存在分子间作用力,所以异硫氰酸的沸点高于硫氰酸,
故答案为:异硫氰酸;
(5)图A体心立方密堆积,晶胞中Fe原子数目为1+8×$\frac{1}{8}$=2,晶胞棱长长度为$\frac{4r}{\sqrt{3}}$cm,图B为面心立方密堆积,晶胞中Fe原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞棱长长度为$\frac{\sqrt{2}}{2}$×4r=2$\sqrt{2}$r cm,晶胞质量之比为2:4=1:2,则A、B两种晶体密度之比是$\frac{1}{(\frac{4r}{\sqrt{3}})^{3}}$:$\frac{2}{(2\sqrt{2r})^{3}}$=$\frac{3\sqrt{6}}{8}$,
故答案为:$\frac{3\sqrt{6}}{8}$.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、杂化方式、配合物、氢键、晶胞计算等,(3)中配位键判断为易错点,(5)中掌握均摊法进行晶胞计算,需要学生具备一定的数学计算能力.

| A. | 分子式为C5H12的烃有3种同分异构体 | |
| B. | 已知丙烷的二氯代物有4种同分异构体,则其六氯代物的同分异构体数目也为4种 | |
| C. | 含有5碳原子的饱和链烃,其一氯代物只有3种 | |
| D. | 菲的结构为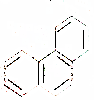 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
| A. | 当V=10时,c(Na+)>c(OH-)>c(HC0${\;}_{3}^{-}$)>c(CH3COO-)>c(H+) | |
| B. | 当 0<V<20 时,c(H+)+c(Na+)=c(HC0${\;}_{3}^{-}$)+c(CH3COO-)+2 c(C032-)+c(OH-) | |
| C. | 当 V=20 时,c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 当 V=40 时,c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 3:1 |
甲$\stackrel{OH-}{→}$乙$\stackrel{H+}{→}$甲.
| A. | Fe2+ | B. | Al | C. | HCO${\;}_{3}^{-}$ | D. | CO2 |
| A. | v(D)=0.05mol/(L•min) | B. | 3v(B)=2v(C) | ||
| C. | v(B)=0.15mol/(L•min) | D. | A的转化率为40% |
 .
.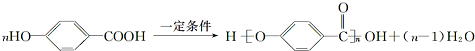 .
.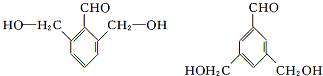 (任意一种).
(任意一种).
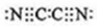 ,(yz)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是2NaOH+(CN)2=NaCN+NaCNO+H2O.
,(yz)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是2NaOH+(CN)2=NaCN+NaCNO+H2O. .
.