题目内容
11.用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,下列关于产物的说法中正确的是( )| A. | 18O存在于乙酸乙酯中 | |
| B. | 生成的乙酸乙酯的相对分子质量为88 | |
| C. | 18O既存在于乙酸乙酯中,又存在于水中 | |
| D. | 18O存在于水中 |
分析 羧酸与醇的酯化反应是可逆的,该反应也属于取代反应;羧酸跟醇的反应过程为:羧酸分子中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯,即酸去羟基醇去羟基氢,据此判断含有18O的化合物,并计算出生成的乙酸乙酯的相对分子量.
解答 解:乙酸与乙醇反应乙酸提供羟基,醇提供羟基氢原子,结合生成水,其余部分互相结合成酯,所以CH3CH218OH与乙酸反应方程式为:CH3COOH+CH3CH218OH CH3CO18OCH2CH3+H2O,由于酯化反应是可逆反应,故乙醇仍存在,故18O只存在于乙醇和乙酸乙酯中,故A正确,C、D错误;
CH3CO18OCH2CH3+H2O,由于酯化反应是可逆反应,故乙醇仍存在,故18O只存在于乙醇和乙酸乙酯中,故A正确,C、D错误;
生成的乙酸乙酯为:CH3CO18OCH2CH3,该酯的相对分子质量为90,故B错误;
故选A.
点评 本题考查酯化反应的原理与特点,难度不大,注意羧酸跟醇的反应过程一般是:羧酸分子中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯.

练习册系列答案
相关题目
1.下列各组中从左到右金属性逐渐减弱的一组是( )
| A. | 钠、镁、铝 | B. | 钠、钾、铷 | C. | 银、汞、铜 | D. | 铁、镁、钠 |
2.已知反应A+B=C+D为吸热反应,对这个反应的下列说法中正确的是( )
| A. | A和B的总能量一定高于C和D的总能量 | |
| B. | A的能量一定低于C的,B的能量一定低于D的 | |
| C. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| D. | 破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量 |
19.已知自然界中氢的同位素有H、D、T三种,氯元素的同位素有 3517Cl和3717Cl两种,试估算自然界的氯化氢最多有( )
| A. | 2种 | B. | 3种 | C. | 6种 | D. | 9种 |
6.下列各种有机物在常温下呈气态的是( )
①苯;②甲醛;③丁烷;④己烷;⑤甲醇;⑥乙烯.
①苯;②甲醛;③丁烷;④己烷;⑤甲醇;⑥乙烯.
| A. | ①③⑤ | B. | ②③④ | C. | ①④⑤ | D. | ②③⑥ |
16.铅蓄电池是典型的可充电池,在现代生活中有着广泛的应用,其充电、放电按下式进行:Pb+PbO2+2H2SO4$\frac{\underline{\;放电\;}}{充电}$2PbSO4+2H2O,有关该电池的说法正确的是( )
| A. | 放电时,负极质量减少 | |
| B. | 放电一段时间后,溶液的pH值减小 | |
| C. | 充电时,阳极反应:PbSO4+2e-=Pb+SO42- | |
| D. | 充电时,铅蓄电池的负极与外接电源的负极相连 |
3.下列反应中,属于加成的是( )
| A. | C2H5OH $→_{170℃}^{浓H_{2}SO_{4}}$ C2H4↑+H2O | |
| B. | 2CH3CHO+O2 $\stackrel{催化剂}{→}$2CH3COOH | |
| C. | CH3-CH=CH2+Br2→CH3-CHBr-CH2Br | |
| D. |  +Br2 $\stackrel{Fe}{→}$ +Br2 $\stackrel{Fe}{→}$ 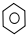 -Br+HBr -Br+HBr |
1.化学科学需要借助化学专用语言来描述,下列化学用语的书写正确的是( )
| A. | Ca2+的结构示意图为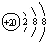 | B. | CO2分子的比例模型示意图: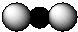 | ||
| C. | 水合钠离子: | D. | 次氯酸的电子式: |