题目内容
某有机物A的结构为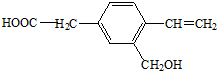 ,下列有关说法正确的是( )
,下列有关说法正确的是( )
 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A、分子式为C10H10O3,是一种芳香烃 |
| B、能发生加聚反应,也能发生酯化反应 |
| C、1 mol A能分别与1 mol金属钠、2mol NaOH反应 |
| D、A分子中所有原子可能在同一平面上 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知,分子中含苯环、碳碳双键、-COOH、-OH,结合苯、烯烃、羧酸、醇的性质来解答.
解答:
解:A.分子中含有O元素,为烃的含氧衍生物,故A错误;
B.分子中含有碳碳双键,可发生加聚反应,含有羧基、羟基,可发生酯化反应,故B正确;
C.A中含有1个羧基、1个羟基,则A能分别与2 mol金属钠、1mol NaOH反应,故C错误;
D.含2个亚甲基,为四面体构型,则不可能所以原子共面,故D错误.
故选B.
B.分子中含有碳碳双键,可发生加聚反应,含有羧基、羟基,可发生酯化反应,故B正确;
C.A中含有1个羧基、1个羟基,则A能分别与2 mol金属钠、1mol NaOH反应,故C错误;
D.含2个亚甲基,为四面体构型,则不可能所以原子共面,故D错误.
故选B.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重羧酸、烯烃、醇性质的考查,注重分析能力与知识综合应用能力的训练,选项D为解答的难点,题目难度不大.

练习册系列答案
相关题目
下列离子方程式中正确的是( )
| A、澄清石灰水与稀盐酸反应Ca(OH) 2+2H+=Ca2++2H2O |
| B、氢氧化钡与硫酸铜溶液混合:Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu (OH) 2↓ |
| C、铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag |
| D、氯化铁溶液与氨水反应Fe3++3OH-=Fe (OH)3↓ |
浓H2SO4能干燥氯气,是利用了浓H2SO4的( )
| A、强酸性 | B、吸水性 |
| C、脱水性 | D、强氧化性 |
在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2中,若有5mol水发生氧化反应,则被还原的BrF3物质的量为( )
| A、2mol | ||
B、
| ||
C、
| ||
| D、5mol |
某有机物的结构简式如图,下列叙述错误的是( )
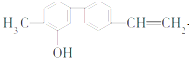

| A、一个分子中含有14个H原子 |
| B、苯环上一氯取代物有2种 |
| C、含有一种含氧官能团 |
| D、分子式是C15H14O |
下列说法正确的是( )
| A、CS2为V形的极性分子 |
| B、电子云示意图中的每个小黑点都表示一个电子 |
| C、非极性键也可以存在于化合物中 |
| D、甲烷、氨和水都是由极性键结合而成的极性分子 |
 二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应: 如图所示的实验装置中,X、Y分别为直流电源的两极.在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入多孔铂电极,切断电源开关S1,合闭开关S2,通直流电一段时间后,请回答下列问题:
如图所示的实验装置中,X、Y分别为直流电源的两极.在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入多孔铂电极,切断电源开关S1,合闭开关S2,通直流电一段时间后,请回答下列问题: