题目内容
下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向AlCl3溶液中加入过量的氨水,过滤,洗涤,干燥,加热灼烧 | 制取Al2O3 |
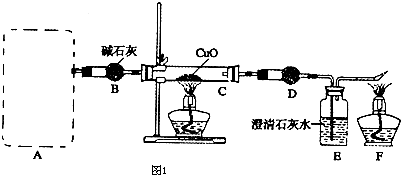
| B | 将浓硫酸与碳混合加热,生成的气体通入足量的澄清石灰水 | 检验气体产物中的CO2 |
| C | 将SO2通入品红溶液中,品红溶液褪色,加热褪色后的品红溶液,溶液恢复红色 | 验证亚硫酸的不稳定性 |
| D | 向某溶液中加入NaOH溶液后再加热,若产生的气体能使湿润的红色石蕊试纸变蓝 | 验证该溶液中肯定有NH4+ |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.向AlCl3溶液中加入过量的氨水,反应生成氢氧化铝沉淀;
B.将浓硫酸与碳混合加热,反应生成二氧化碳和二氧化硫气体;
B.二氧化硫与品红化合生成无色的物质,该物质受热易分解;
D.溶液中加入NaOH溶液后再加热,若产生的气体能使湿润的红色石蕊试纸变蓝,气体为氨气,由N原子守恒分析.
B.将浓硫酸与碳混合加热,反应生成二氧化碳和二氧化硫气体;
B.二氧化硫与品红化合生成无色的物质,该物质受热易分解;
D.溶液中加入NaOH溶液后再加热,若产生的气体能使湿润的红色石蕊试纸变蓝,气体为氨气,由N原子守恒分析.
解答:
解:A.向AlCl3溶液中加入过量的氨水,反应生成氢氧化铝沉淀,则过滤,洗涤,干燥,加热灼烧可生成Al2O3,故A正确;
B.将浓硫酸与碳混合加热,反应生成二氧化碳和二氧化硫气体,均能使石灰水变浑浊,则不能检验气体产物中的CO2,故B错误;
B.二氧化硫与品红化合生成无色的物质,该物质受热易分解,则漂白性与亚硫酸的不稳定无关,故C错误;
D.溶液中加入NaOH溶液后再加热,若产生的气体能使湿润的红色石蕊试纸变蓝,气体为氨气,由N原子守恒可知,该溶液中肯定有NH4+,故D正确;
故选AD.
B.将浓硫酸与碳混合加热,反应生成二氧化碳和二氧化硫气体,均能使石灰水变浑浊,则不能检验气体产物中的CO2,故B错误;
B.二氧化硫与品红化合生成无色的物质,该物质受热易分解,则漂白性与亚硫酸的不稳定无关,故C错误;
D.溶液中加入NaOH溶液后再加热,若产生的气体能使湿润的红色石蕊试纸变蓝,气体为氨气,由N原子守恒可知,该溶液中肯定有NH4+,故D正确;
故选AD.
点评:本题考查化学实验方案的评价,为高频考点,侧重物质性质及化学反应的考查,把握发生的化学反应及现象、结论的关系为解答的关键,注意实验的评价性、操作性分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
化学与人类生活、社会可持续发展密切相关.下列说法不正确的是( )
| A、利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B、催化转化机动车尾气为无害气体,能消除酸雨和雾霾的发生 |
| C、研发高效低毒的农药,降低蔬菜的农药残留量 |
| D、积极开发废电池的综合利用技术,防止电池中的重金属等污染土壤和水体 |
在室温下等体积的酸和碱的溶液,混合后pH值一定小于7的是( )
| A、pH=3的盐酸与pH=11的氨水 |
| B、等物质的量浓度的盐酸与氢氧化钾溶液 |
| C、等物质的量浓度的醋酸与氢氧化钠溶液 |
| D、pH=3的醋酸与pH=11的氢氧化钠溶液 |
 某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A、催化剂能降低该反应的活化能 |
| B、逆反应的活化能大于正反应的活化能 |
| C、该反应为放热反应 |
| D、催化剂能改变该反应的焓变 |
 甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合如图所示.其中甲和X不可能是( )
甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合如图所示.其中甲和X不可能是( )| A、甲为C、X为O2 |
| B、甲为Fe、X为Cl2 |
| C、甲为SO2、X为NH3?H2O |
| D、甲为AlCl3溶液、X为NaOH溶液 |
下列说法中,不正确的是( )
| A、在元素周期表里,元素所在主族的族序数等于其原子核外最外层电子数 |
| B、在元素周期表里,元素所在的周期数等于原子电子层数 |
| C、最外层电子数为8的微粒是稀有气体元素的原子 |
| D、同主族元素的原子序数越大,其原子半径越大 |
乳制品富含钙,紫菜富含铁.这里的“钙”和“铁”指的是( )
| A、分子 | B、元素 | C、单质 | D、氧化物 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,17g甲基(-14CH3)所含的中子数为9NA |
| B、标准状况下,11.2L苯中含有的碳碳双键数为1.5NA |
| C、42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| D、5.6g铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA |