题目内容
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,17g甲基(-14CH3)所含的中子数为9NA |
| B、标准状况下,11.2L苯中含有的碳碳双键数为1.5NA |
| C、42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| D、5.6g铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.甲基(-14CH3)中含有8个中子,17g该甲基的物质的量为1mol,含有8mol中子;
B.标准状况下,苯的状态不是气体,不能使用标况下的气体摩尔体积计算苯的物质的量;
C.乙烯和丙烯的最简式为CH2,根据混合物的最简式计算出含有的碳原子数目;
D.先判断过量情况,然后根据不足量计算出转移的电子数.
B.标准状况下,苯的状态不是气体,不能使用标况下的气体摩尔体积计算苯的物质的量;
C.乙烯和丙烯的最简式为CH2,根据混合物的最简式计算出含有的碳原子数目;
D.先判断过量情况,然后根据不足量计算出转移的电子数.
解答:
解:A.17g甲基(-14CH3)的物质的量为1mol,1mol该甲基中含有8mol中子,所含的中子数为8NA,故A错误;
B.标况下苯不是气体,不能使用标况下的气体摩尔体积计算11.2L苯的物质的量,故B错误;
C.42g乙烯和丙烯的混合物中含有3mol最简式CH2,含有3mol碳原子,含有的碳原子数为3NA,故C正确;
D.5.6g铁的物质的量为0.1mol,0.1mol氯气完全反应消耗0.15mol氯气,氯气不足,反应转移的电子的物质的量为0.2mol,转移的电子数为0.2NA,故D错误;
故选C.
B.标况下苯不是气体,不能使用标况下的气体摩尔体积计算11.2L苯的物质的量,故B错误;
C.42g乙烯和丙烯的混合物中含有3mol最简式CH2,含有3mol碳原子,含有的碳原子数为3NA,故C正确;
D.5.6g铁的物质的量为0.1mol,0.1mol氯气完全反应消耗0.15mol氯气,氯气不足,反应转移的电子的物质的量为0.2mol,转移的电子数为0.2NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下苯不是气体、甲基(-14CH3)中含有的中子数为8,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.

练习册系列答案
相关题目
下列关于化学反应速率的说法,错误的是( )
| A、化学反应速率通常用单位时间内反应物浓度的增加量或生成物浓度的减少量来表示 |
| B、化学反应速率的数值无负值,均为正值 |
| C、不能用固体或纯液体的浓度变化量表示化学反应速率 |
| D、化学反应速率的单位是mol/(L?s)或mol/(L?min) |
下列各组离子在水溶液中能大量共存的是( )
| A、Cu2+、H+、SO42- |
| B、Ba2+、NO3-、CO32- |
| C、Al3+、H+、CO32- |
| D、OH-、Fe2+、NO3- |
一定条件将C5H12裂解,最多可以得到烯烃的种数是( )
| A、3种 | B、4种 | C、5种 | D、6种 |
今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是( )
| A、若a=b,pH(NaX)>pH(NaY),则相同浓度时,酸性HX<HY |
| B、若a=b,并测得c(X-)=c(Y-)+c(HY),则相同浓度时,酸性HX>HY |
| C、若a>b,测得c(X-)=c(Y-),则可推出溶液中c(HX)>c(HY),且相同浓度时,酸性HX>HY |
| D、若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则可推出a+b=0.2mol/L |
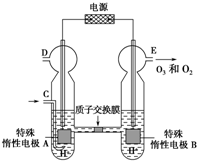 臭氧O3是常用消毒剂,实验室可用电解稀硫酸制备,装置如图(已知溶液中放电顺序:O2>H+).下列说法正确的是( )
臭氧O3是常用消毒剂,实验室可用电解稀硫酸制备,装置如图(已知溶液中放电顺序:O2>H+).下列说法正确的是( )| A、若C处通入O2,电解时溶液中的质子由A极向B极迁移 | ||||
| B、若C处通入O2,A极的电极反应式为:2H++2e-═H2↑ | ||||
C、若C处不通入O2,该制备过程总反应的化学方程式为:3O2
| ||||
D、若C处不通入O2,D、E处分别收集到x L和y L气体(标准状况下),则E处收集的y L气体中O3所占的体积分数为
|
复印机工作时会产生一种腥臭味的气体,该气体只由氧元素组成,其化学式为( )
| A、O2 |
| B、NO2 |
| C、O3 |
| D、N2O |
100.0mL 6.0mol?L-1 H2SO4(aq)跟足量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成H2的总量,可向反应物中加入适量的( )
| A、Na2CO3(s) |
| B、水 |
| C、K2SO4(aq) |
| D、(NH4)2SO4(s) |