题目内容
在室温下等体积的酸和碱的溶液,混合后pH值一定小于7的是( )
| A、pH=3的盐酸与pH=11的氨水 |
| B、等物质的量浓度的盐酸与氢氧化钾溶液 |
| C、等物质的量浓度的醋酸与氢氧化钠溶液 |
| D、pH=3的醋酸与pH=11的氢氧化钠溶液 |
考点:pH的简单计算,水的电离
专题:电离平衡与溶液的pH专题
分析:A.一水合氨为弱电解质,两溶液混合后氨水过量,溶液显示碱性;
B.氯化氢和氢氧化钾都是强电解质,等浓度、等体积的二者混合后溶液显示中性;
C.醋酸为弱酸,等浓度、等体积的醋酸和氢氧化钠溶液混合后恰好反应生成醋酸钠,醋酸根离子水解溶液显示碱性;
D.醋酸为弱电解质,两溶液混合后醋酸过量,溶液显示酸性.
B.氯化氢和氢氧化钾都是强电解质,等浓度、等体积的二者混合后溶液显示中性;
C.醋酸为弱酸,等浓度、等体积的醋酸和氢氧化钠溶液混合后恰好反应生成醋酸钠,醋酸根离子水解溶液显示碱性;
D.醋酸为弱电解质,两溶液混合后醋酸过量,溶液显示酸性.
解答:
解:A.pH=3的盐酸中氢离子浓度为0.001mol/L,而pH=11的氨水中一水合氨的浓度远远大于0.001mol/L,所以两溶液混合后氨水过量,溶液显示碱性,溶液的pH>7,故A错误;
B.盐酸为一元强酸,氢氧化钾为一元强碱,两溶液等浓度、等体积混合后溶液显示中性,溶液的pH=7,故B错误;
C.醋酸为由于弱酸,而氢氧化钠为一元强碱,两溶液等体积、等浓度混合后恰好生成醋酸钠溶液,醋酸根离子水解,溶液显示碱性,溶液的pH>7,故C错误;
D.pH=3的氢氧化钠的浓度为0.001mol/L,而pH=11的醋酸中醋酸的浓度远远大于0.001mol/L,所以两溶液混合后醋酸过量,溶液显示酸性,溶液的pH<7,故D正确;
故选D.
B.盐酸为一元强酸,氢氧化钾为一元强碱,两溶液等浓度、等体积混合后溶液显示中性,溶液的pH=7,故B错误;
C.醋酸为由于弱酸,而氢氧化钠为一元强碱,两溶液等体积、等浓度混合后恰好生成醋酸钠溶液,醋酸根离子水解,溶液显示碱性,溶液的pH>7,故C错误;
D.pH=3的氢氧化钠的浓度为0.001mol/L,而pH=11的醋酸中醋酸的浓度远远大于0.001mol/L,所以两溶液混合后醋酸过量,溶液显示酸性,溶液的pH<7,故D正确;
故选D.
点评:本题考查了酸碱混合后的定性判断及溶液酸碱性与溶液pH的简单计算,题目难度中等,注意掌握溶液酸碱性与溶液pH的计算方法,选项A、D为易错点,注意明确混合液中弱电解质过量.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
在化学能与电能的转化过程中,下列叙述正确的是( )
| A、教材所示的铜-锌原电池在工作时,H+、Zn2+向铜片附近迁移 |
| B、电解饱和食盐水时,阳极得到Cl2和NaOH(aq) |
| C、电解铝时,电解槽里的负极材料发生氧化反应 |
| D、原电池与电解池连接后,电子从原电池负极流向电解池阳极 |
化学反应速率受外界条件如反应温度、反应物浓度、压强、催化剂等的影响.烧烤时,用扇子向红热的木炭扇风,火会更旺,其原因是( )
| A、压强降低,反应减慢 |
| B、温度降低,反应加快 |
| C、使CO2浓度增加,反应加快 |
| D、使O2浓度增加,反应加快 |
下列有关混合物的分离方法中,正确的是( )
| A、从食盐溶液中获得食盐晶体采用蒸发的方法 |
| B、除去酒精中含有的少量水采用萃取的方法 |
| C、将碘晶体中含有的少量沙子除去采用蒸馏的方法 |
| D、从碘水中获得碘的晶体采用过滤的方法 |
下列化学方程式书写正确的是( )
| A、CH3COONa+CO2+H2O→CH3COOH+NaHCO3 | ||||
B、CH3COOH+CH318OH
| ||||
C、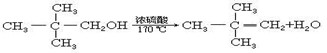 | ||||
D、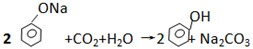 |
下列各组离子在水溶液中能大量共存的是( )
| A、Cu2+、H+、SO42- |
| B、Ba2+、NO3-、CO32- |
| C、Al3+、H+、CO32- |
| D、OH-、Fe2+、NO3- |
 根据物质结构与性质的关系,请回答下列问题:
根据物质结构与性质的关系,请回答下列问题: