题目内容
14.某溶液中加入铝粉能产生氢气,在该溶液中可能大量共存的离子组是( )| A. | SiO32- K+ Fe3+ Cl- | B. | NO3- K+ Mg2+ SO42- | ||
| C. | ClO- Na+ HCO3- SCN- | D. | SO42- Mg2+ Cl- H+ |
分析 加入铝粉能产生氢气,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应、相互促进水解等,则离子大量共存,以此来解答.
解答 解:加入铝粉能产生氢气,为非氧化性酸或强碱溶液,
A.酸性溶液中不能大量存在SiO32-,碱性溶液中不能大量存在 Fe3+,且SiO32-、Fe3+相互促进水解,不能共存,故A不选;
B.酸溶液中Al、NO3-发生氧化还原反应不生成氢气,碱性溶液中不能大量存在Mg2+,故B不选;
C.酸溶液中不能大量存在ClO-、HCO3-,碱溶液中不能大量存在 HCO3-,故C不选;
D.酸溶液中该组离子之间不反应,可大量共存,故D选;
故选D.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.生活因化学而精彩,化学因实验而生动,实验因“洗涤”而更加精准,关于沉淀或晶体洗涤的说法错误的是( )
| A. | 洗净的检验是检验最后一次洗涤液中是否含有形成沉淀的该溶液中的离子 | |
| B. | 洗涤的试剂一般可选用蒸馏水、冰水、乙醇、该物质的饱和溶液 | |
| C. | 洗涤的目的一般是除去沉淀或晶体表面可溶性的杂质,提高纯度 | |
| D. | 洗涤的操作是向过滤器里加洗涤剂,一般洗涤剂尽量多加,然后让洗涤剂自然流下 |
9. 某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
(1)取冰醋酸配制250mL 0.4mol/L的醋酸溶液,用0.4mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示.则稀释过程中溶液的pH由大到小的顺序a>c>b(填字母).
②配制250mL 0.4mol/L 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250mL容量瓶.
③为标定该醋酸溶液的准确浓度,用0.2000mol/L的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
该醋酸溶液的准确浓度为0.2000 mol/L(保留小数点后四位),上述标定过程中,造成测定结果偏高的原因可能是ad(多选、错选不得分).
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
①根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是0.0100 mol/L 醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于l.
②简述用pH试纸测 0.1mol/L 醋酸溶液pH的方法:用镊子取一小片pH试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,与标准比色卡对照.
(3)常温下,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+)<氢氧化钠溶液中c(OH-)(选填“>”或“<”或“=”).
(4)若25℃时CH3COOH的电离平衡常数Ka=1.8×10-5 mol•L-1,向a L CH3COOH溶液中加入bmolCH3COONa,混合液恢复至25℃时呈中性,则原CH3COOH溶液的浓度为$\frac{b}{180a}$mol•L-1.
 某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.(1)取冰醋酸配制250mL 0.4mol/L的醋酸溶液,用0.4mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示.则稀释过程中溶液的pH由大到小的顺序a>c>b(填字母).
②配制250mL 0.4mol/L 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250mL容量瓶.
③为标定该醋酸溶液的准确浓度,用0.2000mol/L的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
②简述用pH试纸测 0.1mol/L 醋酸溶液pH的方法:用镊子取一小片pH试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,与标准比色卡对照.
(3)常温下,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+)<氢氧化钠溶液中c(OH-)(选填“>”或“<”或“=”).
(4)若25℃时CH3COOH的电离平衡常数Ka=1.8×10-5 mol•L-1,向a L CH3COOH溶液中加入bmolCH3COONa,混合液恢复至25℃时呈中性,则原CH3COOH溶液的浓度为$\frac{b}{180a}$mol•L-1.
19.“2015•8•12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.已知部分弱酸的电离平衡常数如下表:
(1)根据价键规则,写出H2CO3的结构式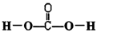 .
.
(2)下列能用于判断氮、碳两种元素非金属性强弱的是abcd(填序号)
a.气态氢化物的稳定性强弱 b.最高价氧化物对应水化物酸性强弱
c.Al2O3+N2+3C=2AlN+3CO d.比较在周期表中的位置
(3)0.01mol/L的NaCN溶液pH=9,用离子方程式表示呈碱性的原因CN-+H2O?HCN+OH-. 请判断该溶液中:c(CN-) c(OH-)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大,处理该污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-.CNO-在酸性条件下继续被NaClO氧化生成N2与CO2.某环保部门用下图装置进行实验,以证明该处理方法的有效性并测定CN-被处理的百分率.
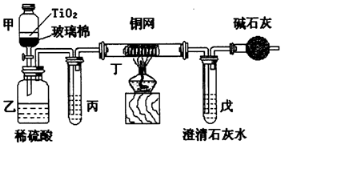
将浓缩后含CN-的废水与过量NaClO溶液的混合液(其中CN-浓度为0.05mol/L)200ml倒入甲中,塞上橡皮塞,一段时间后,打开活塞,使溶液全部放入乙中,关闭活塞.
①甲中反应的离子方程式为CN-+ClO-=CNO-+Cl-,乙中反应的离子方程式为2CNO-+3ClO-+2H+=N2↑+2CO2↑+H2O+3Cl-.
②上述实验是通过测定CO2的量来确定CN-的处理效果.若丙中的试剂是饱和食盐水,且丙、丁都是除杂装置,则乙中产生的气体除CO2、N2外,还可能含有的杂质气体是HCl、Cl2,戊中盛有足量的石灰水,若实验后戊中生成0.9g沉淀,则CN-被处理的百分率为90%.
(5)装置中碱石灰的作用是防止空气中的CO2进入戊,影响对产物的测定.
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
 .
.(2)下列能用于判断氮、碳两种元素非金属性强弱的是abcd(填序号)
a.气态氢化物的稳定性强弱 b.最高价氧化物对应水化物酸性强弱
c.Al2O3+N2+3C=2AlN+3CO d.比较在周期表中的位置
(3)0.01mol/L的NaCN溶液pH=9,用离子方程式表示呈碱性的原因CN-+H2O?HCN+OH-. 请判断该溶液中:c(CN-) c(OH-)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大,处理该污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-.CNO-在酸性条件下继续被NaClO氧化生成N2与CO2.某环保部门用下图装置进行实验,以证明该处理方法的有效性并测定CN-被处理的百分率.

将浓缩后含CN-的废水与过量NaClO溶液的混合液(其中CN-浓度为0.05mol/L)200ml倒入甲中,塞上橡皮塞,一段时间后,打开活塞,使溶液全部放入乙中,关闭活塞.
①甲中反应的离子方程式为CN-+ClO-=CNO-+Cl-,乙中反应的离子方程式为2CNO-+3ClO-+2H+=N2↑+2CO2↑+H2O+3Cl-.
②上述实验是通过测定CO2的量来确定CN-的处理效果.若丙中的试剂是饱和食盐水,且丙、丁都是除杂装置,则乙中产生的气体除CO2、N2外,还可能含有的杂质气体是HCl、Cl2,戊中盛有足量的石灰水,若实验后戊中生成0.9g沉淀,则CN-被处理的百分率为90%.
(5)装置中碱石灰的作用是防止空气中的CO2进入戊,影响对产物的测定.
3.根据价层电子对互斥模型,判断下列分子或者离子的空间构型不是三角锥形的是( )
| A. | PCl3 | B. | H3O+ | C. | NO3- | D. | PH3 |
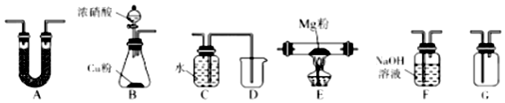
4.下列叙述中错误的是( )
| A. | 消除散落在地上的汞珠的方法是撒上硫粉 | |
| B. | 铜丝擦亮后伸入到硫蒸气产物是CuS | |
| C. | 可以用CS2浸泡的方法除去附在玻璃器皿上的硫 | |
| D. | 可以用加热浓NaOH溶液除去附在试管内壁上的硫 |
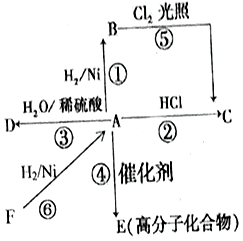 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应.
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应.