题目内容
9. 某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.(1)取冰醋酸配制250mL 0.4mol/L的醋酸溶液,用0.4mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示.则稀释过程中溶液的pH由大到小的顺序a>c>b(填字母).
②配制250mL 0.4mol/L 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250mL容量瓶.
③为标定该醋酸溶液的准确浓度,用0.2000mol/L的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
②简述用pH试纸测 0.1mol/L 醋酸溶液pH的方法:用镊子取一小片pH试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,与标准比色卡对照.
(3)常温下,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+)<氢氧化钠溶液中c(OH-)(选填“>”或“<”或“=”).
(4)若25℃时CH3COOH的电离平衡常数Ka=1.8×10-5 mol•L-1,向a L CH3COOH溶液中加入bmolCH3COONa,混合液恢复至25℃时呈中性,则原CH3COOH溶液的浓度为$\frac{b}{180a}$mol•L-1.
分析 (1)①导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
②实验一配制步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,根据配制一定物质的量浓度溶液的步骤以及仪器的用途选取仪器;
③根据NaOH的体积,第3次数据显然误差较大,舍去;另外三次所用NaOH平均体积为20 mL,代入计算;根据c(待测)=$\frac{V(标准)×c(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差;
(2)①部分电离的电解质是弱电解质;
②根据pH试纸的使用方法回答,用镊子取一小片pH试纸放在表面皿(或玻璃片)上,用蘸有待测溶液的玻璃棒点在试纸的中部测定溶液PH;
(3)醋酸为弱电解质,溶液中部分电离出氢离子,等体积的两溶液混合pH=7,若m=n,溶液显示中性,则醋酸浓度稍大;
(4)向a L CH3COOH溶液中加入bmolCH3COONa,混合液恢复至25℃时呈中性,c(H+)=c(OH-)=10-7mol/L,电荷守恒得到c(Na+)+c(H+)=c(OH-)+c(CH3COO-),得到c(Na+)=c(CH3COO-)=$\frac{b}{a}$mol.L,结合电力平衡常数计算;
解答 解:(1)①导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH由大到小为a>c>b,
故答案为:a>c>b;
②实验一配制步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用量筒量取冰醋酸,把冰醋酸倒入烧杯进行溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要玻璃仪器有玻璃棒、烧杯、胶头滴管、250mL容量瓶、量筒,故答案为:250mL容量瓶;
③根据NaOH的体积,第3次数据显然误差较大,舍去;另外三次所用NaOH平均体积为20 mL,
则氢氧化钠溶液平均浓度=$\frac{0.2000mol/L×0.02L}{0.02L}$=0.200 0 mol•L-1,
a.未用标准液润洗碱式滴定管,消耗标准溶液体积大,测定结果偏大,故a正确;
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确,读取标准溶液体积减小,测定结果偏低,故b错误;
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗,对测定结果无影响,故c错误;
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液,读取标准溶液体积会增大,测定结果会偏大,故d正确;
故选ad,
故答案为:0.2000 mol/L;ad;
(2)①孤立的看每次测量值,H+浓度远小于醋酸的浓度,说明醋酸不完全电离;联系起来看,浓度为0.100 0 mol•L-1、0.010 0 mol•L-1及0.001 0 mol•L-1的醋酸,pH变化值小于1,所以醋酸是弱电解质,
故答案为:0.010 0 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1;
②pH试纸的正确使用方法是:用镊子取一小片pH试纸放在表面皿(或玻璃片)上,用蘸有待测溶液的玻璃棒点在试纸的中部,试纸变色后,与标准比色卡比较来确定溶液的pH;
故答案为:用镊子取一小片pH试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,与标准比色卡对照;
(3)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,当m=n时,两溶液恰好反应生成醋酸钠,溶液显示碱性,若使溶液的pH=7,则醋酸的浓度应该稍大一些,即m>n;由于醋酸为弱酸,则溶液中氢离子浓度小于氢氧化钠溶液中氢氧根离子浓度,即c(H+)<氢氧化钠溶液中c(OH-),
故答案为:<;
(4)向a L CH3COOH溶液中加入bmolCH3COONa,混合液恢复至25℃时呈中性,c(H+)=c(OH-)=10-7mol/L,电荷守恒得到c(Na+)+c(H+)=c(OH-)+c(CH3COO-),得到c(Na+)=c(CH3COO-)=$\frac{b}{a}$mol.L,Ka=1.8×10-5 mol•L-1=$\frac{c(C{H}_{3}CO{O}^{-})c({H}^{+})}{c(C{H}_{3}COOH)}$=$\frac{\frac{b}{a}mol/L×1{0}^{-7}mol/l}{c(C{H}_{3}COOH)}$,c(CH3COOH)=$\frac{b}{180a}$mol/L,
故答案为:$\frac{b}{180a}$;
点评 本题考查了弱电解质的电离及实验探究、弱电解质的电离特点、电离平衡常数、守恒思想分析计算、溶液配制和误差分析等知识点,掌握基础注意积累是解题关键,题目难度中等.

| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 1:3 |
①Fe(+2)②Fe(+3)③S(-1)④O(0)⑤S(+4)
| A. | ①和③ | B. | 只有④ | C. | 只有③ | D. | 只有① |
| A. | SiO32- K+ Fe3+ Cl- | B. | NO3- K+ Mg2+ SO42- | ||
| C. | ClO- Na+ HCO3- SCN- | D. | SO42- Mg2+ Cl- H+ |
| A. | 硬铝 | B. | 青铜 | C. | 不锈钢 | D. | 水银 |
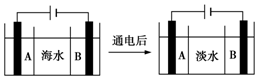 水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.
水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.