题目内容
下列物质的用途,利用氧化还原反应的是( )
| A、用氯气消毒浴池 |
| B、用稀盐酸除去热水瓶胆壁上的水垢(主要成分是CaCO3) |
| C、用食盐腌渍食物 |
| D、用小苏打治疗胃酸过多 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:利用氧化还原反应,说明该反应中有电子转移,其特征是有元素化合价升降,据此分析解答.
解答:
解:A.利用氯气消毒,发生的反应为Cl2+H2O=HCl+HClO,该反应Cl元素化合价由0价变为-1价和+1价,所以发生氧化还原反应,次氯酸具有强氧化性而细菌消毒,故A正确;
B.发生的反应为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应中没有元素化合价升降,所以不属于氧化还原反应,但属于复分解反应,故B错误;
C.利用水自由扩散原理,食盐水使细菌脱水死亡而防止变质,但没有电子转移,所以不属于氧化还原反应,故C错误;
D.发生的反应为NaHCO3+HCl=NaCl+H2O+CO2↑,该反应中没有元素化合价升降,所以不属于氧化还原反应,但属于复分解反应,故D错误;
故选A.
B.发生的反应为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应中没有元素化合价升降,所以不属于氧化还原反应,但属于复分解反应,故B错误;
C.利用水自由扩散原理,食盐水使细菌脱水死亡而防止变质,但没有电子转移,所以不属于氧化还原反应,故C错误;
D.发生的反应为NaHCO3+HCl=NaCl+H2O+CO2↑,该反应中没有元素化合价升降,所以不属于氧化还原反应,但属于复分解反应,故D错误;
故选A.
点评:本题考查氧化还原反应,明确氧化还原反应本质是解本题关键,知道氧化还原反应的本质和特征区别,知道常见元素化合价,题目难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
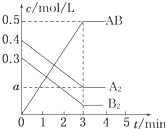 一定条件下,在一个容积为2L的密闭容器中加入0.8mol A2气体和0.6mol B2气体反应达平衡生成1mol AB气体并释放出热量,反应中各物质的浓度随时间的变化情况如图所示.下列说法不正确的是( )
一定条件下,在一个容积为2L的密闭容器中加入0.8mol A2气体和0.6mol B2气体反应达平衡生成1mol AB气体并释放出热量,反应中各物质的浓度随时间的变化情况如图所示.下列说法不正确的是( )| A、图中a点的值为0.15 |
| B、该反应的平衡常数K=0.03 |
| C、温度升高,平衡常数K值减小 |
| D、平衡时A2的转化率为62.5% |
下列现象或应用不能用胶体知识解释的是( )
| A、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
| B、长江三角洲的形成 |
| C、氯化铝溶液中加入NaOH溶液会产生白色沉淀 |
| D、盐水点豆腐 |
反应4NH3+5O2?4NO+6H2O在一定体积的密闭容器中进行,30s后NO的物质的量浓度增加了3mol/L,则下列反应速率正确的是( )
| A、v (NO)=0.02 mol?(L?s)-1 |
| B、v (NO)=0.2mol?(L?s)-1 |
| C、v (NH3)=0.01 mol?(L?s)-1 |
| D、v (NH3)=0.1 mol?(L?s)-1 |
下列基本实验操作中,不合理的是( )
| A、配制一定物质的量浓度溶液,向容量瓶加水至离刻度线1~2cm时,改用胶头滴管定容 |
| B、可用湿润的pH试纸检验氨气 |
| C、用洁净的铂丝蘸取待测溶液,置于火焰上灼烧,透过蓝色钴玻璃能观察到火焰呈紫色,该溶液中一定含有钾离子,不含有钠离子 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
测定稀盐酸和氢氧化钠稀溶液中和热的实 验中没有使用的仪器有:①大、小烧杯;②容量瓶;③量筒;④环形玻璃搅拌棒;⑤试管;⑥温度计;⑦蒸发皿;⑧托盘天平中的( )
| A、②⑤⑦⑧ | B、①②⑥⑦ |
| C、②③⑦⑧ | D、③④⑤⑦ |
要鉴别己烯中是否混有少量甲苯,正确的实验方法是( )
| A、点燃这种液体,然后观察火焰的颜色 |
| B、先加足量酸性高锰酸钾溶液,然后再加入溴水 |
| C、加入浓硫酸与浓硝酸后加热 |
| D、先加足量溴水,然后再加入酸性高锰酸钾溶液 |