题目内容
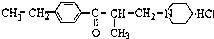 盐酸乙哌立松片是一种骨骼肌松弛剂,能改善由肩周炎、腰痛症等引起的肌紧张状况,其结构筒式如图:关于盐酸乙哌立松片有下列说法其中正确的是( )
盐酸乙哌立松片是一种骨骼肌松弛剂,能改善由肩周炎、腰痛症等引起的肌紧张状况,其结构筒式如图:关于盐酸乙哌立松片有下列说法其中正确的是( )①是芳香族化合物
②含有N原子的六元环上所有原子均处于同一平面
③能发生还原反应
④是一种有机盐.
| A、①③④ | B、①②③ |
| C、①②④ | D、②③④ |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:该有机物含苯环、C=O、及-HCl结构,结合有关的概念及酮的性质来解答.
解答:
解:①该物质含苯环,属于芳香族化合物,故①正确;
②含有N原子的六元环上,5个C均为四面体结构,则不可能所有原子均处于同一平面,故②错误;
③含C=O,能与氢气发生加成反应,属于还原反应,故③正确;
④含-HCl结构,则为盐酸盐,属于有机盐,故④正确;
故选A.
②含有N原子的六元环上,5个C均为四面体结构,则不可能所有原子均处于同一平面,故②错误;
③含C=O,能与氢气发生加成反应,属于还原反应,故③正确;
④含-HCl结构,则为盐酸盐,属于有机盐,故④正确;
故选A.
点评:本题考查有机物的结构与性质,为高考常见题型,明确常见有机物的官能团是解答的关键,注意加H的反应为还原反应及盐的判断,题目难度不大.

练习册系列答案
相关题目
下列各组离子在指定溶液中一定能大量共存的是( )
| A、能使甲基橙呈红色的溶液:Ba2+、Al3+、NO3-、Cl- |
| B、由水电离出的c(H+)=1×10-11 mol?L-1溶液:Na+、Mg2+、Cl-、NO3- |
| C、0.2 mol?L-1的NaNO3溶液:H+、Fe2+、SO42-、Cl- |
| D、与Fe反应生成H2的溶液:NH4+、K+、SO42-、CO32- |
设NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A、室温下,1mol SO3含有的分子数为NA个 |
| B、0.1molAl3+离子含有核外电子数为NA个 |
| C、1molCl2与1mol Fe反应,转移电子为3 NA个 |
| D、标准状况下2.24L己烷含有分子数目为0.1 NA个 |
下列实验与所得结论相符的是( )
| A、将碘水倒入分液漏斗,加适量乙醇,震荡后静置,能将碘萃取到乙醇中 |
| B、用湿润的pH试纸测定溶液的pH,测定结果偏小,该溶液一定呈酸性 |
| C、向某溶液中加入K3[Fe(CN)6]溶液,生成特征蓝色的沉淀,原溶液中含有Fe2+ |
| D、在含有FeCl2杂质的FeCl3溶液中通入足量的Cl2后,充分加热蒸干,可得到纯净的FeCl3 |
实验是研究化学的基础,下列图中所示的实验方法、装置或操作中正确的是( )
A、 制备乙酸乙酯 制备乙酸乙酯 |
B、 测定中和热 |
C、 测定反应速率 |
D、 分离溴乙烷和水 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol N2所含有的原子数为NA |
| B、标准状况下,22.4 L水中含有的水分子数为NA |
| C、标准状况下,22.4 L氯化氢所含的原子数为NA |
| D、32 g O2所含的氧原子数目为2NA |
下列离子方程式书写正确的是( )
| A、在硫氢化钠溶液中加入稀硫酸溶液:S2-+2H+→H2S↑ |
| B、用氢氧化钠溶液除去镁粉中的铝粉:2Al+2OH-→AlO2-+H2↑ |
| C、向碳酸氢钠溶液中加入少量氢氧化钙溶液:2HCO3-+Ca2++2OH-→CaCO3↓+CO32-+2H2O |
| D、偏铝酸钠溶液中通入少量二氧化碳:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |

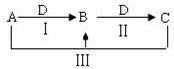 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).