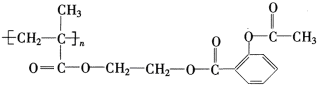题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol N2所含有的原子数为NA |
| B、标准状况下,22.4 L水中含有的水分子数为NA |
| C、标准状况下,22.4 L氯化氢所含的原子数为NA |
| D、32 g O2所含的氧原子数目为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氮气为双原子分子,1mol氮气中含有2mol氮原子;
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.氯化氢为双原子分子,1mol氯化氢中含有2mol原子;
D.氧气为双原子分子,1mol氧气中含有2mol氧原子.
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.氯化氢为双原子分子,1mol氯化氢中含有2mol原子;
D.氧气为双原子分子,1mol氧气中含有2mol氧原子.
解答:
解:A.氮气分子含有2个氮原子,所以1mol N2含有2mol氮原子,含有的原子数为2NA,故A错误;
B.标准状况下,水不是气体,不能适用于气体摩尔体积进行计算,故B错误;
C.氯化氢含有2个原子,所以标准状况下,22.4 L氯化氢的物质的量为1mol,所含的原子数为2NA,故C错误;
D.32g氧气的物质的量是1mol,所以含有2mol氧原子,所含的氧原子数目为2NA,故D正确;
故选D.
B.标准状况下,水不是气体,不能适用于气体摩尔体积进行计算,故B错误;
C.氯化氢含有2个原子,所以标准状况下,22.4 L氯化氢的物质的量为1mol,所含的原子数为2NA,故C错误;
D.32g氧气的物质的量是1mol,所以含有2mol氧原子,所含的氧原子数目为2NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,题目难度不大,注意掌握标况下气体摩尔体积的使用条件,明确物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
对于相同体积的K2CO3溶液(浓度为c1)和(NH4)2CO3溶液(浓度为c2),若其中CO32-的物质的量浓度相同,则c1和c2的关系是( )
| A、c1=c2 |
| B、c1>c2 |
| C、c1≥c2 |
| D、c1<c2 |
烧过菜的铁锅未及时洗涤,会出现红棕色锈斑.整个过程不可能发生的变化为( )
| A、2H2O+O2+4e-═4OH- |
| B、Fe-3e-═Fe3+ |
| C、Fe2++2OH-═Fe(OH)2 |
| D、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
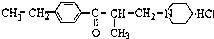 盐酸乙哌立松片是一种骨骼肌松弛剂,能改善由肩周炎、腰痛症等引起的肌紧张状况,其结构筒式如图:关于盐酸乙哌立松片有下列说法其中正确的是( )
盐酸乙哌立松片是一种骨骼肌松弛剂,能改善由肩周炎、腰痛症等引起的肌紧张状况,其结构筒式如图:关于盐酸乙哌立松片有下列说法其中正确的是( )①是芳香族化合物
②含有N原子的六元环上所有原子均处于同一平面
③能发生还原反应
④是一种有机盐.
| A、①③④ | B、①②③ |
| C、①②④ | D、②③④ |
下列有关钢铁腐蚀的叙述正确的是( )
| A、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
| B、与铜质水龙头连接处的钢质水管不易发生腐蚀 |
| C、可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| D、在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,关于该元素的说法正确的是( )
| A、在自然界中既有化合态又有游离态 |
| B、单质常用作半导体材料 |
| C、气态氢化物很稳定 |
| D、最高价氧化物不与任何酸反应,可制光导纤维 |
下列实验中没有颜色变化的是( )
| A、蔗糖溶液中加入稀硫酸 |
| B、鸡蛋清中加入浓硝酸 |
| C、淀粉溶液中加入碘酒 |
| D、麦芽糖溶液与新制的Cu(OH)2浊液混合加热 |
 )具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式:
)具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式: