题目内容
在标准状况下,将aLNH3完全溶于水得到V mL氨水,溶液的密度为ρg·cm-3,溶质的质量分数为ω,溶质的物质的量浓度为Cmol/L。下列叙述中正确的是
①ω=
②C=
③上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
④上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为: c(Cl-) > c(NH4+) > c(H+) > c(OH-)
A、①④ B、②③ C、①③ D、②④
D
【解析】
试题分析:①溶液中氨气的质量是aL/22.4L/mol×17g/mol=17a/22.4g,溶液的质量是VmL×ρg·cm-3=ρVg,所以溶质的质量分数为ω=17a/22.4g÷ρVg×100%=17a/22.4ρV×100%,错误;②根据物质的量浓度的定义C=n/V=aL/22.4L/mol/V×10-3L=1000a/22.4Vmol/L,正确;③,因为氨水的密度比水小,所以加入VmL水后,VmL水的质量大于VmL氨水的质量,则氨水的质量分数小于0.5ω,错误;④上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液为氯化铵和氯化氢的等浓度的混合液,溶液呈酸性,所以溶液中离子浓度的大小关系是c(Cl-) > c(NH4+) > c(H+) > c(OH-),正确,所以答案选D。
考点:考查溶液的物质的量浓度的计算、物质的量浓度与质量分数的关系,溶液稀释的计算

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
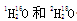 。下列有关说法正确的是
。下列有关说法正确的是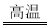 CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。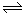 2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是
2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是