题目内容
向100mL0.1mol/L的氢氧化钠溶液中缓慢通入一定量的CO2气体,下列有关反应后的溶液说法错误的是( )
| A、该溶液中一定存在:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
| B、该溶液中可能存在:c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
| C、向该溶液中滴入少量稀盐酸,一定会产生气泡 |
| D、向该溶液中滴入少量Ca(OH)2溶液,一定会有白色沉淀产生 |
考点:离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:A.无论是碳酸钠溶液还是碳酸氢钠,溶液中一定满足电荷守恒,根据电荷守恒进行判断;
B.当氢氧化钠与二氧化碳按照物质的量1:1反应,反应后的溶液为碳酸氢钠溶液,根据碳酸氢钠溶液中电荷守恒和物料守恒进行判断;
C.若二氧化碳不足,反应后的溶液组成为碳酸钠溶液或碳酸钠、氢氧化钠的混合物,则加入盐酸后不会生成气体;
D.碳酸钠、碳酸氢钠都能够与氢氧化钙反应生成碳酸钙沉淀.
B.当氢氧化钠与二氧化碳按照物质的量1:1反应,反应后的溶液为碳酸氢钠溶液,根据碳酸氢钠溶液中电荷守恒和物料守恒进行判断;
C.若二氧化碳不足,反应后的溶液组成为碳酸钠溶液或碳酸钠、氢氧化钠的混合物,则加入盐酸后不会生成气体;
D.碳酸钠、碳酸氢钠都能够与氢氧化钙反应生成碳酸钙沉淀.
解答:
解:A.溶液中一定遵循电荷守恒,根据电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故A正确;
B.氢氧化钠与二氧化碳可以反应生成碳酸氢钠溶液,碳酸氢钠溶液中,根据物料守恒可得:①c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),根据电荷守恒可得:②c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),将①带入②可得:c(H+)+c(H2CO3)=c(OH-)+c(CO32-),故B正确;
C.当二氧化碳不足、氢氧化钠过量时,反应后溶液中的溶质为Na2CO3溶液或Na2CO3、NaOH的混合物,则加入盐酸后不会生成气体,故C错误;
D.NaOH溶液与二氧化碳反应后的溶液中,溶质组成可能为:Na2CO3与NaOH的混合物、Na2CO3、Na2CO3与NaHCO3的混合物、NaHCO3,无论那种情况,加入氢氧化钙后都会生成碳酸钙沉淀,故D正确;
故选C.
B.氢氧化钠与二氧化碳可以反应生成碳酸氢钠溶液,碳酸氢钠溶液中,根据物料守恒可得:①c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),根据电荷守恒可得:②c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),将①带入②可得:c(H+)+c(H2CO3)=c(OH-)+c(CO32-),故B正确;
C.当二氧化碳不足、氢氧化钠过量时,反应后溶液中的溶质为Na2CO3溶液或Na2CO3、NaOH的混合物,则加入盐酸后不会生成气体,故C错误;
D.NaOH溶液与二氧化碳反应后的溶液中,溶质组成可能为:Na2CO3与NaOH的混合物、Na2CO3、Na2CO3与NaHCO3的混合物、NaHCO3,无论那种情况,加入氢氧化钙后都会生成碳酸钙沉淀,故D正确;
故选C.
点评:本题考查离子浓度的大小比较,为高考常见题型,侧重于学生分析能力的考查,题目难度中等,注意从电荷守恒和物料守恒的角度分析该题,选项C为易错点,注意分析反应后溶液中溶质的组成情况.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
图表是元素周期表中短周期的一部分.A、D两元素原子核内质子数之和为23.下列有关说法中不正确的是( )
| A | B | |
| C | D |
| A、原子半径:A>B |
| B、C的最简单氢化物的分子构型为平面三角形 |
| C、最高价氧化物对应水化物的酸性:D>C |
| D、SiO2可溶解在溶有HB的溶液中 |
“化学是一门中心学科,与社会、生活有密切的关系”.下列叙述中正确的是( )
| A、液化石油气的主要成分是甲烷 |
| B、不锈钢餐具和目前流通的硬币都属于合金 |
| C、医院给病人做X光透视时,常给病人服用“钡餐”,其主要成分是碳酸钡 |
| D、制作航天服的聚酯纤维和用于通讯光缆的光导纤维都是新型无机非金属材料 |
下列各组离子在指定溶液中,能大量共存的是( )
| A、强碱性溶液中:K+,ClO-,Ba2+,Cl- |
| B、水电离c(H+)═10-12mol?L-1的溶液中:Cl-,CO32-,NO3-,NH4+ |
| C、使甲基橙变红的溶液中:Fe2+,MnO4-,NO3-,Na+ |
| D、中性溶液中:Al3+,NO3-,Cl-,S2- |
电浮选凝聚法处理酸性污水的工作原理如图.下列说法不正确的是( )

| A、铁电极发生的电极反应式为:Fe-2e-=Fe2+ |
| B、通入甲烷的电极反应式为:CH4+4CO32--8e-=5CO2+2H2O |
| C、为增强污水的导电能力,可向污水中加入适量工业用食盐 |
| D、若左池石墨电极产生44.8L(标况)气体,则消耗0.5 mol氧气 |
鉴别甲苯、苯酚溶液、已烯、碘化钾淀粉溶液、硝酸银溶液等五种无色液体的一种试剂是( )
| A、KMnO4酸性溶液 |
| B、FeCl3溶液 |
| C、溴水 |
| D、金属钠 |
 工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个的关键步骤.
工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个的关键步骤.
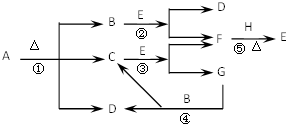 已知化合物A、D、E、G进行焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多.A~H各物质的变化关系如图所示.
已知化合物A、D、E、G进行焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多.A~H各物质的变化关系如图所示.