题目内容
11.下列关于浓硫酸的说法错误的是( )| A. | 能干燥氯气 | B. | 能使蔗糖炭化 | ||
| C. | 久置后浓度变大 | D. | 加热时能与碳反应 |
分析 A、浓硫酸具有吸水性,氯气和浓硫酸不反应,可以干燥;
B、浓硫酸具有脱水性,可以使蔗糖脱水;
C、浓硫酸具有吸水性,可以吸收空气中的水蒸气;
D、浓硫酸具有强氧化性加热条件下和碳反应生成二氧化碳、二氧化硫和水;
解答 解:A、浓硫酸具有吸水性,氯气和浓硫酸不反应,能干燥氯气,故A正确;
B、浓硫酸具有脱水性,可以使蔗糖脱水发生炭化现象,故B正确;
C、浓硫酸具有吸水性,可以吸收空气中的水蒸气,久置后浓度变小,故C错误;
D、浓硫酸具有强氧化性加热条件下和碳反应生成二氧化碳、二氧化硫和水,故D正确;
故选C.
点评 本题考查了浓硫酸性质分析,浓硫酸具有吸水性,能吸收空气里的水蒸气,且浓硫酸溶于水时放出大量的热.浓硫酸具有强氧化性,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列说法正确的是( )
| A. | 盐类发生水解的过程中,溶液的pH一定发生改变 | |
| B. | 向K2CO3溶液中通入CO2可使溶液中的c(CO32-)变大 | |
| C. | 向Na2SO3溶液中通入Cl2,溶液的导电性变强 | |
| D. | 一定温度下的密闭容器中,反应2NO2?N2O4达平衡时,再加入1molN2O4,平衡正向移动,且N2O4含量增大 |
19.下列各组离子,能在指定溶液中一定能大量共存的是( )
| A. | 含有大量Fe3+的溶液:Na+、SCN-、Cl-、I- | |
| B. | 中性溶液:Fe3+、Al3+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ | |
| C. | 常温下,pH=12的溶液:Na+、K+、Cl-、SO${\;}_{4}^{2-}$ | |
| D. | 与铝粉反应放出H2的无色溶液:Br-、Al3+、Na+、SO${\;}_{4}^{2-}$ |
16.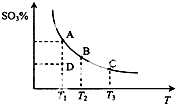 二氧化硫的催化氧化原理为2SO2(g)+O2(g)?2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
二氧化硫的催化氧化原理为2SO2(g)+O2(g)?2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
 二氧化硫的催化氧化原理为2SO2(g)+O2(g)?2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
二氧化硫的催化氧化原理为2SO2(g)+O2(g)?2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )| A. | 在D点时v正>v逆 | |
| B. | 其他条件不变,增大氧气的浓度可以提高二氧化硫的转化率 | |
| C. | 若B、C点的平衡常数分别为KB、KC,则KB>KC | |
| D. | 恒温恒容下向平衡体系中通入氦气,平衡向右移动 |
3.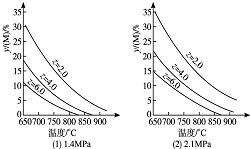 反应aM(g)+bN(g)?cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如图所示.其中z表示反应开始时N的物质的量与M的物质的量之比.下列说法不正确的是( )
反应aM(g)+bN(g)?cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如图所示.其中z表示反应开始时N的物质的量与M的物质的量之比.下列说法不正确的是( )
 反应aM(g)+bN(g)?cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如图所示.其中z表示反应开始时N的物质的量与M的物质的量之比.下列说法不正确的是( )
反应aM(g)+bN(g)?cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如图所示.其中z表示反应开始时N的物质的量与M的物质的量之比.下列说法不正确的是( )| A. | 同温同压同z时,加入催化剂,平衡时Q的体积分数不改变 | |
| B. | 同温同压时,增加z,平衡时Q的体积分数一定增加 | |
| C. | 同温同z时,增加压强,平衡时Q的体积分数一定减小 | |
| D. | 同压同z时,升高温度,平衡时Q的体积分数一定增加 |
20.在密闭容器中,A和B反应生成C,其反应速率分别用v(A)、v (B)、v (C)表示,已知它们之间的如下关系:3v (A)=2v (B),3v (C)=2v (B).则此反应可表示为( )
| A. | 3A+2B=2C | B. | 2A+3B=2C | C. | 3A+2B=3C | D. | A+B=C |