��Ŀ����
5���Ŵ�����������ڵ��£�������ȱ���Ļ����У���Ȼ��ʴ���أ��绯ѧ��ʴ����ԭ����һ�ֽ��������λ�ԭ����ϸ�������ṩ������Ӧ�Ĵ�����ÿ48gSO42-�ŵ�ת�Ƶ�����Ϊ2.408��1024���÷�Ӧ�ų�����������ϸ����������ֳ֮�裮��д���õ绯ѧ��ʴ��������Ӧ�ĵ缫��Ӧʽ��SO42-+8e-+4H2O�TS2-+8OH-
���������ǰ����������ĸ�ʴ��������У�д��ѧʽ��Fe��OH��2��FeS��
���� ��ԭ��ص����������õ��ӵĻ�ԭ��Ӧ�������е�SO42-��ԭΪS2-���Դ���д�缫��Ӧʽ��
����������ĸ�ʴ��������ʴ���������ӻ��������֮�䷢����Ӧ���ݴ˻ش�
��� �⣺�������е�SO42-��ԭΪS2-����֪�õ����ӣ���õ缫��ӦʽΪSO42-+4H2O+8e-=S2-+8OH-���ʴ�Ϊ��SO42-+8e-+4H2O�TS2-+8OH-��
����������ĸ�ʴ��������ʴ�������Ͻ�����ʧ���ӣ�����������Ӧ�������������ӣ����������ϻ����Fe��OH��2��ͬʱ�����е�SO42-��ԭΪS2-�����������ӽ��ΪFeS���ʴ�Ϊ��Fe��OH��2��FeS��
���� ���⿼��ѧ��ԭ���ԭ����Ӧ��֪ʶ��ע��缫��Ӧʽ����д�ǽ���Ĺؼ����Ѷ��еȣ�

��ϰ��ϵ�д�
 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
�����Ŀ
15��������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ������ͼ��ʾ������˵����ȷ���ǣ�������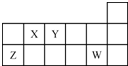

| A�� | ԭ�Ӱ뾶�Ĵ�С˳��rZ��rY��rX | |
| B�� | Y�ļ��⻯��ˮ��Һ������ | |
| C�� | Y���⻯����W���⻯�ﲻ�ܷ�����Ӧ | |
| D�� | X��Y��Z��W����Ԫ�ص�����������Ӧˮ���������ǿ�Ӧ |
16��Ϊ�ⶨ��ʽ̼����[Cox��OH��y��CO3��z]�Ļ�ѧ��ɣ��о���ѧϰС���ͬѧ�������ͼ��ʾ��װ�ý���ʵ��̽������֪����ʽ̼��������ʱ�ɷֽ��������������
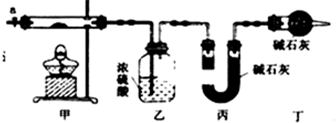
��1������ͼ��ʾװ����װ�������������װ�������ԣ���ȡ3.65g��Ʒ����Ӳ�ʲ������ڣ����ȣ�����װ���в��������ݲ���ʱ��װ���У���ʵ������ֹͣ���ȣ�����a������ͨ����������ӣ�ͨ�������Ŀ�������ɵ�CO2��H2O��g��ȫ�������ҡ���װ�ã�
��2��ijͬѧ��Ϊ����ʵ���д���һ��ȱ�ݣ���ȱ����δ���ǿ����е�ˮ�����Ͷ�����̼��ʵ���Ӱ�죮
��3��ͨ����ȷʵ�����ҡ���װ�����طֱ�Ϊ0.36g��0.88g����ü�ʽ̼���ܵĻ�ѧʽΪCo3��OH��4��CO3��2��
��4��CoCl2•6H2O���������ˮ������Ӽ����Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2•6H2O��һ�ֹ������£�
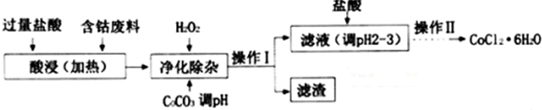
��֪��25��ʱ
�پ�������ʱ������H2O2������Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O��
�ڼ���CoCO3��pHΪ5.2��7.6�������I��õ������ɷ�ΪFe��OH��3��Al��OH��3��
�ۼ��������pHΪ2��3��Ŀ��Ϊ����CoCl2��ˮ�⣮

��1������ͼ��ʾװ����װ�������������װ�������ԣ���ȡ3.65g��Ʒ����Ӳ�ʲ������ڣ����ȣ�����װ���в��������ݲ���ʱ��װ���У���ʵ������ֹͣ���ȣ�����a������ͨ����������ӣ�ͨ�������Ŀ�������ɵ�CO2��H2O��g��ȫ�������ҡ���װ�ã�
��2��ijͬѧ��Ϊ����ʵ���д���һ��ȱ�ݣ���ȱ����δ���ǿ����е�ˮ�����Ͷ�����̼��ʵ���Ӱ�죮
��3��ͨ����ȷʵ�����ҡ���װ�����طֱ�Ϊ0.36g��0.88g����ü�ʽ̼���ܵĻ�ѧʽΪCo3��OH��4��CO3��2��
��4��CoCl2•6H2O���������ˮ������Ӽ����Ժ��ܷ��ϣ�������Fe��Al�����ʣ���ȡCoCl2•6H2O��һ�ֹ������£�

��֪��25��ʱ
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 |
| ��ʼ������pH | 2.3 | 7.5 | 7.6 | 3.4 |
| ��ȫ������pH | 4.1 | 9.7 | 9.2 | 5.2 |
�ڼ���CoCO3��pHΪ5.2��7.6�������I��õ������ɷ�ΪFe��OH��3��Al��OH��3��
�ۼ��������pHΪ2��3��Ŀ��Ϊ����CoCl2��ˮ�⣮
13���������ʵķе��ɸߵ������е��ǣ�������
��CH3��CH2��2CH3
��CH3��CH2��3CH3
�ۣ�CH3��3CH
�ܣ�CH3��2CHCH2CH3��
��CH3��CH2��2CH3
��CH3��CH2��3CH3
�ۣ�CH3��3CH
�ܣ�CH3��2CHCH2CH3��
| A�� | �ܢڢ٢� | B�� | �ڢܢ٢� | C�� | �ܢ٢ڢ� | D�� | �ڢܢۢ� |
20���л���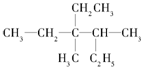 ����ȷ����Ϊ��������
����ȷ����Ϊ��������
 ����ȷ����Ϊ��������
����ȷ����Ϊ��������| A�� | 3-��4��4-���һ����� | B�� | 3-��3��4-���һ����� | ||
| C�� | 4-��2��2-���һ����� | D�� | 3��4-����3-�һ����� |
17��ij��������̼���⡢������Ԫ����ɣ���������ͼ��C-H����O-H����C-O���������գ����л������Է���������60������л���Ľṹ��ʽ��������
| A�� | CH3CH2OCH3 | B�� | CH3CH��OH��CH3 | C�� | CH3CH2 CH2CH2OH | D�� | CH3CH2CHO |
14����������0.1mol/L�����¼�����Һ����H2SO4��Һ����NaHSO4��Һ����CH3COOH��Һ����HCl��Һ����HCN��Һ����NH3•H2O�����������¼�����Һ�ĵ���ȣ����Ѿ������ռԭ���ܵİٷ������������֪H2SO4�ĵ�һ����������ȫ�ģ����ش��������⣺
��1�������£�pH��ͬ�ı����м�����Һ�������ʵ���Ũ���ɴ�С��˳���ǣ�����ţ���ͬ���ۣ��ڣ��ܣ��٣�
��2�������£���������п��Ͷ������pH=1�ı����м�����Һ�У�����H2�������ͬ��ͬѹ�£��ɴ�С��˳���Ǣۣ��ڣ��٣��ܣ�
��3����25��ʱ��������֪Ũ�ȵ�NaOH�ζ�δ֪Ũ�ȵ�CH3COOHӦѡ�÷�̪��ָʾ�������յ�ʱ��ҺpH=a������ˮ�����c��H+��Ϊ10��a-14��mol/L��
��4����25��ʱ����bmol•L-1��KCN��Һ��0.01mol•L-1������������ϣ���Ӧ�ﵽƽ��ʱ�������ҺpH=7����KCN��Һ�����ʵ���Ũ��b��0.01mol•L-1���������������=�������ú�b�Ĵ���ʽ��ʾHCN�ĵ��볣��Ka=��100b-1����10-7 mol•L-1��
| ��H2SO4��Һ��HSO4- | ��NaHSO4��Һ��HSO4- | ��CH3COOH | ��HCl��Һ |
| 10% | 29% | 1.33% | 100% |
��2�������£���������п��Ͷ������pH=1�ı����м�����Һ�У�����H2�������ͬ��ͬѹ�£��ɴ�С��˳���Ǣۣ��ڣ��٣��ܣ�
��3����25��ʱ��������֪Ũ�ȵ�NaOH�ζ�δ֪Ũ�ȵ�CH3COOHӦѡ�÷�̪��ָʾ�������յ�ʱ��ҺpH=a������ˮ�����c��H+��Ϊ10��a-14��mol/L��
��4����25��ʱ����bmol•L-1��KCN��Һ��0.01mol•L-1������������ϣ���Ӧ�ﵽƽ��ʱ�������ҺpH=7����KCN��Һ�����ʵ���Ũ��b��0.01mol•L-1���������������=�������ú�b�Ĵ���ʽ��ʾHCN�ĵ��볣��Ka=��100b-1����10-7 mol•L-1��
 ��ʾ�ķ���ʽC7H12��������3-��-2��4-����ϩ��
��ʾ�ķ���ʽC7H12��������3-��-2��4-����ϩ��