题目内容
CO,CH4均为常见的可燃气体.
(1)等体积的CO,CH4在相同的条件下分别完全燃烧,转移的电子数之比为______.
(2)120℃,101kPa下,a mL由CO,CH4组成的混合气体在b mL氧气中完全燃烧后,恢复至原来的温度与压强.
①若混合气体与氧气恰好完全反应,产生b mLCO2,则混合气体中CH4的体积分数为______%.
②若燃烧后气体体积缩小了a/4mL,则a与b的关系为______数学表达式表示).
解:(1)一个CO转移的电子数为2,一个CH4转移的电子数为8,等体积的CO,CH4转移的电子数之比为1:4,故答案为:1:4;
(2)①设CO为xml,CH4为yml,
2CO+O2 2CO2
2CO2
xml xml
xml
CH4 +2O2 CO2+2H2O
CO2+2H2O
yml 2yml yml
则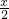 +2y=a,x+y=a
+2y=a,x+y=a
解得:x= ,y=
,y=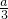 ,
,
所以混合气体中CH4的体积分数为 ×100%=33.3%;
×100%=33.3%;
②设CO为xml,CH4为yml,
2CO+O2 2CO2 △V
2CO2 △V
xml xml
xml 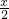 ml
ml
CH4 +2O2 CO2+2H2O
CO2+2H2O
yml 2yml yml
则 ①x+y=a;
② +2y≤b
+2y≤b
③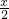 =
=
由③得,可得到a=2x,代入①式,可得到:y=x=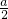 ,代入②式,可得到b≥
,代入②式,可得到b≥ ,故答案为:b≥
,故答案为:b≥ ;
;
分析:(1)根据CO反应后生成CO2,碳的价态由+2升高到+4价,化合价升高2,即一个CO转移的电子数为2,CH4反应后生成CO2和水,碳的价态由-4升高到+4价,化合价升高8,即一个CH4转移的电子数为8来分析计算;
(2)①根据方程式2CO+O2 2CO2、CH4+2O2
2CO2、CH4+2O2 CO2+2H2O,建立方程式组求解;
CO2+2H2O,建立方程式组求解;
②根据方程式2CO+O2 2CO2、CH4+2O2
2CO2、CH4+2O2 CO2+2H2O,利用差量法,建立方程式组求解;
CO2+2H2O,利用差量法,建立方程式组求解;
点评:本题主要考查了利用化学方程式进行计算,难度不大,注意找出各个量之间的关系.
(2)①设CO为xml,CH4为yml,
2CO+O2
 2CO2
2CO2xml
 xml
xml CH4 +2O2
 CO2+2H2O
CO2+2H2Oyml 2yml yml
则
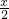 +2y=a,x+y=a
+2y=a,x+y=a解得:x=
 ,y=
,y=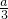 ,
,所以混合气体中CH4的体积分数为
 ×100%=33.3%;
×100%=33.3%;②设CO为xml,CH4为yml,
2CO+O2
 2CO2 △V
2CO2 △Vxml
 xml
xml 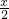 ml
mlCH4 +2O2
 CO2+2H2O
CO2+2H2O yml 2yml yml
则 ①x+y=a;
②
 +2y≤b
+2y≤b ③
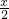 =
=
由③得,可得到a=2x,代入①式,可得到:y=x=
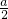 ,代入②式,可得到b≥
,代入②式,可得到b≥ ,故答案为:b≥
,故答案为:b≥ ;
;分析:(1)根据CO反应后生成CO2,碳的价态由+2升高到+4价,化合价升高2,即一个CO转移的电子数为2,CH4反应后生成CO2和水,碳的价态由-4升高到+4价,化合价升高8,即一个CH4转移的电子数为8来分析计算;
(2)①根据方程式2CO+O2
 2CO2、CH4+2O2
2CO2、CH4+2O2 CO2+2H2O,建立方程式组求解;
CO2+2H2O,建立方程式组求解;②根据方程式2CO+O2
 2CO2、CH4+2O2
2CO2、CH4+2O2 CO2+2H2O,利用差量法,建立方程式组求解;
CO2+2H2O,利用差量法,建立方程式组求解;点评:本题主要考查了利用化学方程式进行计算,难度不大,注意找出各个量之间的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目