题目内容
下列指定反应的离子方程式正确的是
A.将铜插入浓硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
B.向FeBr2溶液中通入过量氯气:2Fe2++Cl2=2Fe3++2Cl-
C.向Al2O3中加入氨水:Al2O3+2OH-=2 AlO2-+H2O
D.碳和浓硫酸加热:C+2H++SO42-=H2O+ SO2↑+ CO2↑
练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
短周期元素W、X、Y、Z的原子序数依次增加。m、n、p是由这些元素组成的二元化合物,W2、X2、Z2分别是元素W、X、Z的单质。已知:
I.一定条件下某密闭容器中可发生反应:aX2+bW2 cm,反应过程中物质的浓度变化如下:
cm,反应过程中物质的浓度变化如下:
| X2 | W2 | m |
起始浓度/mol·L-1 | 0.4 | 0.4 | 0 |
平衡浓度/mol·L-1 | 0.3 | 0.1 | 0.2 |
II.它们可发生如下反应:2m(g)+3Z(g)=6n(g)+X2(g);4n(g)+Y2(g) 2p(l)+2Z2(g)。
2p(l)+2Z2(g)。
下列说法正确的是
A.原子半径:W<X<Y B.a:b:c=3:1:2
C.X的氧化物一定是无色气体 D.m、n、p三种物质均为共价化合物
6.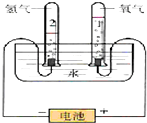 水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
(1)写出电解水的化学方程式,若为氧化还原反应,请用双线桥表示出电子的转移方向和数目.
 .
.
(2)假设电解了3.6gH2O,请完成下表.
(3)若在47.8gH2O(过量)中加入2.3gNa.钠与水反应的离子方程式为2Na+2 H2O═2Na++2OH-+H2↑,,反应后得到的溶液中溶质是NaOH,溶质的质量分数为8%,若要计算该溶液中溶质的物质的量浓度,则还需要溶液密度(填物理量).
(4)若在电解水后收集到O2体积为22.4mL(在标准状况下),则收集到的H2的质量0.004g.
 水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.(1)写出电解水的化学方程式,若为氧化还原反应,请用双线桥表示出电子的转移方向和数目.
 .
.(2)假设电解了3.6gH2O,请完成下表.
| 质 量 | 物质的量 | O2与H2的体积比(同温同压下) | |
| O2 | 3.2g | 0.1mol | 1:2 |
| H2 | 0.4g | 0.2mol |
(4)若在电解水后收集到O2体积为22.4mL(在标准状况下),则收集到的H2的质量0.004g.


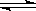 xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
 2C(g)+D(g) △H<0的平衡移动图像,影响平衡移动的原因可能是
2C(g)+D(g) △H<0的平衡移动图像,影响平衡移动的原因可能是


 c”或“d”)
c”或“d”)
 以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 。
以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 。