题目内容
9.①某NaCl样品中可能含有SO42-,CO32-,为检验杂质离子的存在,采取如下实验步骤:样品$\stackrel{溶解}{→}$ $\stackrel{加入足量试剂A}{→}$无明显现象$\stackrel{加入试剂B}{→}$无明显现象.则加入的试剂A为盐酸,B为氯化钡(填化学式),该现象证明样品中不含有CO32-、SO42-.
②在后续实验中需要使用450mL0.5mol•L-1NaCl溶液,为配制该浓度NaCl溶液进行实验,需用托盘天平称取NaCl14.6g.
③配制NaCl溶液时,若出现下列操作,会使配制浓度偏高的是BC
A.称量时NaCl已潮解
B.天平砝码已锈蚀
C.定容时俯视刻度线
D.定容摇匀后液面下降,又加水至刻度.
分析 ①用稀盐酸检验碳酸根的存在,再用氯化钡检验硫酸根的存在;
②容量瓶的规格没有450mL,应选500mL配制,依据n=cV计算物质的量,再计算出质量;
③分析操作对溶质的物质的量n和溶液的体积V,依据c=$\frac{n}{V}$进行误差分析,凡是使n偏大或者使V偏小的操作,溶液浓度偏高,凡是使n偏小或者V偏大的操作,溶液浓度偏低.
解答 解:①取样品溶解,加入足量稀盐酸,无气泡产生,说明样品中不含碳酸根,再加入氯化钡溶液,无白色沉淀产生,说明溶液中不含硫酸根,
故答案为:盐酸;氯化钡;CO32-、SO42-;
②容量瓶的规格没有450mL,应选500mL配制,则需氯化钠的物质的量为:n=cV=0.50mol/L×0.5L=0.25mol,氯化钠的质量为:m=nM=0.25mol×58.5g/mol=14.625g,托盘天平应保留1位小数,氯化钠的质量为14.6g,
故答案为:14.6;
③A.称量时NaCl已潮解,溶质偏少,浓度偏低,故A错误;
B.天平砝码生锈,所称溶质氯化钠质量偏大,浓度偏高,故B正确;
C.定容时,俯视读取刻度,导致溶液体积偏小,溶液浓度偏高,故C正确;
D.定容摇匀后液面下降,是正常现象,又加水至刻度,导致溶液体积偏大,溶液浓度偏低,故D错误;
故答案为:BC.
点评 本题考查常见离子的检验方法以及一定物质的量浓度溶液配制误差分析,明确配制原理,依据c=$\frac{n}{V}$即可解答,题目难度不大.

练习册系列答案
相关题目
5.用已知物质的量浓度的盐酸滴定待测的氢氧化钠溶液,下列情况会使滴定结果偏高的是( )
| A. | 酸式滴定管用水洗净后未用标准液润洗 | |
| B. | 锥形瓶内有水珠未干燥就加入待测的氢氧化钠溶液 | |
| C. | 滴定终点时俯视滴定管读数 | |
| D. | 滴定时溶液刚变成无色就立即停止滴定 |
20.化学反应速率与限度与生产、生活密切相关
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3min,原因是该反应是放热反应,此时温度高,反应速率越大.
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率0.025mol/(L•min).
(设溶液体积不变)
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是CD.
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,3种气态物质 X、Y、Z的物质的量随时间变化曲线如右图.
①该反应的化学方程式是3X+Y?2Z.
②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是CD.
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成1mol Y的同时生成2mol Z
③2min内X的转化率为30%.
④若上述反应中X、Y、Z分别为H2、N2、NH3,且已知17g氨气分解成氮气和氢气要吸收46kJ热量,则该反应的热化学反应方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol.
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率0.025mol/(L•min).
(设溶液体积不变)
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是CD.
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,3种气态物质 X、Y、Z的物质的量随时间变化曲线如右图.

①该反应的化学方程式是3X+Y?2Z.
②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是CD.
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成1mol Y的同时生成2mol Z
③2min内X的转化率为30%.
④若上述反应中X、Y、Z分别为H2、N2、NH3,且已知17g氨气分解成氮气和氢气要吸收46kJ热量,则该反应的热化学反应方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol.
17.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施.化学反应的反应热通常用实验进行测定,也可进行理论推算.
(1)实验测得,5g甲醇(CH3OH)液体在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则表示甲醇标准燃烧热的热化学方程为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)今有如下两个热化学方程式:?则a>b(填“>”、“=”或“<”)
2H2(g)+O2(g)═2H2O(g)△H1=a kJ•mol-1?
2H2(g)+O2(g)═2H2O(l)△H2=b kJ•mol-1?
(3)
已知反应N2(g)+3H2(g)═2NH3(g)△H=a kJ•mol-1.试根据表中所列键能数据估算a 的值:-93(注明“+”或“-”).
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ•mol-1[
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.3kJ•mol-1
总反应:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g)的△H=-246.4 kJ•mol-1.
(1)实验测得,5g甲醇(CH3OH)液体在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则表示甲醇标准燃烧热的热化学方程为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)今有如下两个热化学方程式:?则a>b(填“>”、“=”或“<”)
2H2(g)+O2(g)═2H2O(g)△H1=a kJ•mol-1?
2H2(g)+O2(g)═2H2O(l)△H2=b kJ•mol-1?
(3)
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ•mol-1[
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.3kJ•mol-1
总反应:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g)的△H=-246.4 kJ•mol-1.
4.为把溴水中溴单质萃取出来,应加入( )
| A. | 苯 | B. | 苯乙烯 | C. | 乙醇 | D. | 1-己炔 |
14.同温同体积同质量的下列气体压强最大的是( )
| A. | CO2 | B. | CH4 | C. | N2 | D. | O2 |
1.100mL 1mol•L-1Al2(SO4)3溶液中,含Al3+离子的物质的量( )
| A. | 0.1mol | B. | 0.2mol | C. | 0.3mol | D. | 0.4mol |
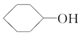 ④
④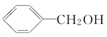 ⑤
⑤