题目内容
在常温下,某溶液中由水电离出的 c(H+)=1×10-11mol?L-1,下列说法正确的是( )
| A、该溶液肯定显碱性 |
| B、该溶液肯定显酸性 |
| C、该溶液的pH可能是11,也可能是3 |
| D、该溶液的pH肯定不是11 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:水存在电离平衡H2O?H++OH-,纯水中水电离的氢离子浓度为:c(H+)=1×10-7mol/L,水电离出的c(H+)=1×10-11 mol/L<1×10-7mol/L,说明抑制了水的电离,该溶液可能为酸和碱,据此进行解答.
解答:
解:水电离出的c(H+)=1×10-13 mol/L<1×10-7mol/L,说明抑制了水的电离,
该溶液可能为酸性或者碱性溶液,故A、B错误;
若为酸性溶液,溶液中氢氧根离子是水电离的,溶液中氢氧根浓度=水电离出的氢离子浓度为:1×10-11 mol/L,溶液的pH=3;若为碱性溶液,则溶液中氢离子是水电离的,溶液的pH为11,故C正确,D错误;
故选C.
该溶液可能为酸性或者碱性溶液,故A、B错误;
若为酸性溶液,溶液中氢氧根离子是水电离的,溶液中氢氧根浓度=水电离出的氢离子浓度为:1×10-11 mol/L,溶液的pH=3;若为碱性溶液,则溶液中氢离子是水电离的,溶液的pH为11,故C正确,D错误;
故选C.
点评:本题考查了水的电离及其影响因素,题目难度中等,注意掌握影响水的电离的因素,明确酸或者碱抑制了水的电离,能够水解的盐促进了水的电离.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列能用或图装置制取气体并能“随开随用、随关随停”的是( )
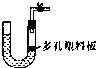

| A、锌粒和稀硫酸制取氧气 |
| B、电石和水制取乙炔 |
| C、浓盐酸和二氧化锰制取氯气 |
| D、大理石和稀硫酸制取二氧化碳 |
下列有关实验室一般事故的预防和处理方法正确的是( )
| A、如果苯酚浓溶液沾到皮肤上,应立即用稀氢氧化钠溶液清洗 |
| B、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 |
| C、不慎将酒精洒到桌面上引起着火,应立即用较多的水浇灭 |
| D、蒸发溶液时有液滴飞溅,应立即加水冷却 |
已知在浓H2SO4存在并加热至140℃的条件下,2个醇分子在羟基上发生分子间脱水反应生成醚,用浓H2SO4跟分子式分别为C2H6O和C3H8O的醇的混合液反应,可得到醚的种类有( )
| A、1种 | B、3种 | C、5种 | D、6种 |
下列关于有机物的叙述正确的是( )
| A、所有含碳元素的化合物都是有机物 |
| B、大多数有机物难溶于有机溶剂 |
| C、熔点低的化合物是有机物 |
| D、有机物中除含碳元素外,还常含有氢、氧等元素 |
化学在生产和日常生活中有着重要的作用.下列说法不正确的是( )
| A、世界各国流通的货币材质一般都是合金,所有的不锈钢中都含有非金属元素 |
| B、在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
| C、工业上用石灰对煤燃烧后形成的烟气进行脱硫,并能回收到石膏 |
| D、电解MgCl2饱和溶液,可制得金属镁,镁合金的硬度和强度均高于纯镁 |
下列热化学方程式能表示可燃物燃烧热的是( )
| A、H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ?mol-1 | ||
| B、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3 kJ?mol-1 | ||
| C、2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ?mol-1 | ||
D、CO(g)+
|
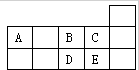 如表为元素周期表短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是( )
如表为元素周期表短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是( )| A、A与B形成的阴离子可能有:AB32-、A2B42- |
| B、E的氢化物的沸点比C的氢化物的沸点低 |
| C、D在过量的B中燃烧的主要产物为DB3 |
| D、这5种元素形成只含极性键的非极性分子多于4种 |
下列说法正确的是( )
| A、pH=3的HX与pH=11的YOH等体积混合,所得溶液的pH一定为7 |
| B、在0.1 mol/L(NH4)2Fe(SO4)2溶液中c(H+)+c(NH4+)+c(Fe2+)=c(OH-)+c(SO42-) |
| C、向醋酸钠溶液中加入适量醋酸,所得酸性溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、0.4 mol/LHCl与0.1 mol/L NaAlO2等体积混合,所得溶液中c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-) |