题目内容
10.某有机物的结构式如图所示,下列关于该有机物的说法正确的是( )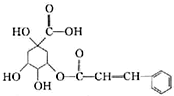
| A. | 分子式为C16H16O7 | |
| B. | 能与钠、乙醇、乙酸、溴发生反应,不能与碳酸钠发生反应 | |
| C. | 能发生取代反应、氧化反应、加成反应,不能发生水解发应 | |
| D. | 1mol 该有机物最多能与2mol NaOH或4mol H2发生反应 |
分析 该物质中含有醇羟基、羧基、酯基、碳碳双键和苯环,具有醇、羧酸、酯、烯烃和苯的性质,能发生消去反应、氧化反应、取代反应、加成反应、水解反应等,据此分析解答.
解答 解:A.根据结构简式知,其分子式为C16H17O7,故A错误;
B.含有羧基,所以能与碳酸钠溶液反应生成二氧化碳,故B错误;
C.含有酯基,所以能发生水解反应,故C错误;
D.碳碳双键和苯环能与氢气发生加成反应,羧基和酯基水解生成的羧基能与NaOH反应,所以1mol 该有机物最多能与2mol NaOH或4mol H2发生反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查醇、羧酸、酯的性质,易错选项是D,注意羧基和酯基不能和氢气发生加成反应.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.反应C(s)+H2O(g)?CO(g)+H2(g)在一个容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加少量的C | |
| B. | 将容器的体积缩小为原来的一半 | |
| C. | 保持体积不变,充入H2使体系压强增大 | |
| D. | 保持压强不变,充入N2使容器体积增大 |
1.根据有机物的系统命名法,下列命名正确的是( )
| A. | 二溴乙烷  | B. | 3-乙基-1-丁烯  | ||
| C. | 2-甲基-2,4-己二烯  | D. | 2,4,4-三甲基戊烷  |
5.下列离子方程式正确的是( )
| A. | 向含有Fe203的悬浊液中通入HI:Fe203+6H+═2Fe3++3H20 | |
| B. | 1 mol/L NaAl02溶液和1.5 mol/L HC1溶液等体积混合:6AlO2-+9H++3H2O═5A1(OH)3+Al3+ | |
| C. | 向Ca( Cl0)2溶液中通入S02:Ca2++2ClO-+S02+H20═CaSO3+2HC1O | |
| D. | 向0.1 mol/LpH=l的NaHA溶液中加入NaOH溶液:HA-+OH-═H2O+A2- |
15.下列过程不涉及氧化还原反应的是( )
| A. |  火法炼铜 | B. |  中和滴定 | C. |  酿酒 | D. |  制眼镜 |
2.下列各粒子:①H3O+、NH${\;}_{4}^{+}$、Na+;②O${\;}_{2}^{2-}$、Na+、Mg2+;③OH-、NH${\;}_{2}^{-}$、F-;④CH4、NH3、H2O.具有相同质子数和电子数的一组是( )
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
19.下列离子方程式正确的是( )
| A. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| B. | SO2通入BaCl2溶液中:Ba2++SO2+H2O=BaSO3↓+2H+ | |
| C. | 硫酸铵溶液与Ba(OH)2溶液反应:Ba2++SO42-=BaSO4↓ | |
| D. | FeCl2溶液与Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
