题目内容
19.下列离子方程式正确的是( )| A. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| B. | SO2通入BaCl2溶液中:Ba2++SO2+H2O=BaSO3↓+2H+ | |
| C. | 硫酸铵溶液与Ba(OH)2溶液反应:Ba2++SO42-=BaSO4↓ | |
| D. | FeCl2溶液与Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
分析 A.Cu与稀硫酸不反应;
B.盐酸的酸性大于亚硫酸;
C.漏写生成一水合氨的离子反应;
D.反应生成氯化铁,遵循电子、电荷守恒.
解答 解:A.Cu与稀硫酸不反应,不能写离子反应,故A错误;
B.盐酸的酸性大于亚硫酸,SO2通入BaCl2溶液中不反应,故B错误;
C.漏写生成一水合氨的离子反应,硫酸铵溶液与Ba(OH)2溶液反应的离子反应为2OH-+2NH4++Ba2++SO42-=BaSO4↓+2NH3.H2O,故C错误;
D.反应生成氯化铁,遵循电子、电荷守恒,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故D正确;
故选D.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
9.居民所用石油液化气的主要成分是丁烷,在使用过程中,常有一些杂质以液态沉积于钢瓶中,这些杂质是( )
| A. | 甲烷和丙烷 | B. | 乙烷和甲醛 | C. | 乙烷和丁烷 | D. | 戊烷和己烷 |
10.某有机物的结构式如图所示,下列关于该有机物的说法正确的是( )
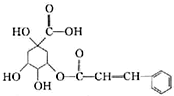

| A. | 分子式为C16H16O7 | |
| B. | 能与钠、乙醇、乙酸、溴发生反应,不能与碳酸钠发生反应 | |
| C. | 能发生取代反应、氧化反应、加成反应,不能发生水解发应 | |
| D. | 1mol 该有机物最多能与2mol NaOH或4mol H2发生反应 |
7.下列各组物质中,所含化学键类型完全相同的是( )
| A. | HCl和MgCl2 | B. | H2O和CO2 | C. | NH4Cl和CCl4 | D. | HCl和NaOH |
11.下列说法正确的是( )
| A. | 在氨水中加入少量的水或氯化铵固体后,都能使溶液中的c(OH-)减小 | |
| B. | 对于反应2SO2(g)+O2(g)?2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 | |
| C. | 25℃下,在NH3•H2O稀溶液中,加水,$\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$的值不变 | |
| D. | 在NaHS溶液中,滴入少量CuCl2溶液产生黑色沉淀,HS-水解程度增大,pH增大 |
8.分别进行如下表所示实验,现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈红色 | 稀硝酸不能将Fe氧化为Fe3+ |
| B | NaAlO2溶液中滴入NaHCO3溶液 | 产生白色沉淀 | AlO2-与HCO3-发生双水解反应 |
| C | 向某溶液里滴加稀NaOH溶液并将湿润的红色石蕊试纸置于试管口 | 试纸颜色没变 | 原溶液中无NH4+ |
| D | 将0.1mol•L-1MgSO4溶液滴入到NaOH溶液里至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液 | 先有白色沉淀生成,后变为蓝色沉淀 | Cu(OH)2的Ksp比Mg(OH)2的Ksp小 |
| A. | A | B. | B | C. | C | D. | D |
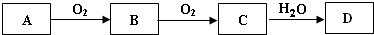
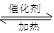 2SO3.
2SO3.