题目内容
 如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )
如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( )| A、甲池b极上析出金属银,乙池c极上析出某金属 |
| B、甲池a极上析出金属银,乙池d极上析出某金属 |
| C、某盐溶液可能是CuSO4溶液 |
| D、某盐溶液可能是Mg(NO3)2溶液 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,甲中a为阴极,b为阳极,银在a极析出,乙中c为阴极,d为阳极,金属在c极析出,乙池电极析出0.24g金属,说明乙池中含有氧化性比氢离子强的金属,以此解答该题.
解答:
解:测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,甲中a为阴极,b为阳极,银在a极析出,乙中c为阴极,d为阳极,金属在c极析出,
A、甲池a极上析出金属银,乙池c极上析出某金属,故A错误;
B、甲池a极上析出金属银,乙池c极上析出某金属,故B错误;
C、乙池电极析出0.24g金属,说明乙池中含有氧化性比氢离子强的金属,则某盐溶液可能是CuSO4溶液,故C正确;
D、Mg2+氧化性较弱,电解时在溶液中不能得电子析出金属,所以某盐溶液不能是Mg(NO3)2溶液,故D正确;
故选C.
A、甲池a极上析出金属银,乙池c极上析出某金属,故A错误;
B、甲池a极上析出金属银,乙池c极上析出某金属,故B错误;
C、乙池电极析出0.24g金属,说明乙池中含有氧化性比氢离子强的金属,则某盐溶液可能是CuSO4溶液,故C正确;
D、Mg2+氧化性较弱,电解时在溶液中不能得电子析出金属,所以某盐溶液不能是Mg(NO3)2溶液,故D正确;
故选C.
点评:本题考查原电池和电解池的工作原理,侧重于电解原理的考查,根据离子的放电顺序解答,题目难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列实验不能达到目的是( )
| A、用NaOH溶液除去镁粉中的铝粉 |
| B、用氯水和KSCN溶液检验Fe2+ |
| C、用盐酸和AgNO3溶液鉴定Cl- |
| D、用加热的方法鉴别Na2CO3和NaHCO3 |
下列叙述正确的是( )
| A、元素的化学性质主要决定于原子的核外电子数 | ||||||
| B、氯化氢溶于水能导电,但液态氯化氢不能导电 | ||||||
C、
| ||||||
| D、导电性强的溶液里自由移动的离子数目一定比导电性弱的溶液里自由移动的离子数目多 |
对于已经达到平衡的可逆反应,下列物理量的变化可以肯定可逆反应平衡发生了移动的是( )
| A、浓度变化 | B、压强变化 |
| C、体积变化 | D、转化率变化 |
下列芳香烃的一氯代物的同分异构体数目最多的是( )
A、 |
B、 |
C、 |
D、 |
扑热息痛是一种优良的解热镇痛剂其结构为 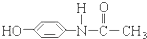 它可能具有的化学性质是( )
它可能具有的化学性质是( )
 它可能具有的化学性质是( )
它可能具有的化学性质是( )| A、不与烧碱溶液反应 |
| B、能与溴水发生取代反应 |
| C、不能被氧化 |
| D、遇FeCl3溶液发生显色反应 |
下列醇中能由醛加氢还原制得的是( )
| A、CH3CH2CH2OH |
| B、(CH3) 2CHCH(CH3) OH |
| C、(CH3) 3COH |
| D、(CH3) 2CHOH |
下列说法不正确的是( )
| A、△H<0且熵增大的反应一定可以自发进行 |
| B、△H>0且熵减小的反应一定不能自发进行 |
| C、△H>0且熵增大的反应一定可以自发进行 |
| D、△H<0且熵减小的反应有可能可以自发进行 |