题目内容
下列反应的离子方程式书写正确的是( )
| A、硫酸铝溶液中加入过量氨水 Al3++30H-═Al(OH)3↓ |
| B、NaHCO3溶液与过量的Ca(OH)2溶液反应 HCO3-+0H-+Ca2+═CaCO3↓+H2O |
| C、碳酸钙与醋酸反应 CaCO3+2H+═Ca2++CO2↑+H2O |
| D、FeI2溶液通入少量Cl2 2Fe2++Cl2═2Fe3++2Cl- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成硫酸氨和氢氧化铝,一水合氨在离子反应中保留化学式;
B.NaHCO3完全反应,生成碳酸钙、水、NaOH;
C.醋酸在离子反应中保留化学式;
D.碘离子还原性强,少量氯气先氧化碘离子.
B.NaHCO3完全反应,生成碳酸钙、水、NaOH;
C.醋酸在离子反应中保留化学式;
D.碘离子还原性强,少量氯气先氧化碘离子.
解答:
解:A.硫酸铝溶液中加入过量氨水的离子反应为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故A错误;
B.NaHCO3溶液与过量的Ca(OH)2溶液反应的离子反应为HCO3-+0H-+Ca2+═CaCO3↓+H2O,故B正确;
C.碳酸钙与醋酸反应的离子反应为CaCO3+2HAc═Ca2++CO2↑+H2O+2Ac-,故C错误;
D.FeI2溶液通入少量Cl2的离子反应为2I-+Cl2═I2+2Cl-,故D错误;
故选B.
B.NaHCO3溶液与过量的Ca(OH)2溶液反应的离子反应为HCO3-+0H-+Ca2+═CaCO3↓+H2O,故B正确;
C.碳酸钙与醋酸反应的离子反应为CaCO3+2HAc═Ca2++CO2↑+H2O+2Ac-,故C错误;
D.FeI2溶液通入少量Cl2的离子反应为2I-+Cl2═I2+2Cl-,故D错误;
故选B.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,选项D为解答的难点,题目难度不大.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、在硫酸亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | ||||
B、MnO2与浓盐酸反应制取Cl2:MnO2+4HCl(浓)
| ||||
| C、过量的KHSO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | ||||
| D、向稀氢氧化钠溶液中通入少量CO2:OH-+CO2═HCO3- |
有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )


| A、①为简单立方堆积 ②为六方最密堆积 ③为体心立方堆积 ④为面心立方最密堆积 |
| B、晶胞中原子的配位数分别为:①6,②8,③8,④12 |
| C、金属镁采取③的堆积方式 |
| D、空间利用率的大小关系为:①<②<③<④ |
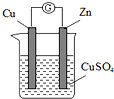 某实验兴趣小组按如图装置实验后,所记录内容合理的是( )
某实验兴趣小组按如图装置实验后,所记录内容合理的是( )| 实验 记录 | ①Cu为正极,Zn为负极; ②Zn质量减少,Cu质量不变; ③SO42- 向Cu极移动; ④电子流方向是:由Zn经导线流入Cu片; ⑤Zn电极发生还原反应; ⑥正极反应式:Cu2++2e-═Cu |
| A、①④⑥ | B、②③④ |
| C、①②⑤ | D、③⑤⑥ |
化学与生产、生活和社会密切相关,下列说法正确的是( )
| A、汽车排放的尾气和燃煤排放颗粒污染物是形成雾霾的重要因素 |
| B、为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
| C、高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| D、“低碳”生活倡导节能减排,禁止使用化石燃料,减少污水排放 |
 熔融状态下,Na和FeCl2能组成可充电电池(装置如图所示),反应原理为:2Na+FeCl2
熔融状态下,Na和FeCl2能组成可充电电池(装置如图所示),反应原理为:2Na+FeCl2| 放电 |
| 充电 |
| A、放电时,a为正极,b为负极 |
| B、放电时,负极反应为:Fe2++2e-=Fe |
| C、充电时,a接外电源正极 |
| D、充电时,b极处发生氧化反应 |
下列叙述正确的是( )
| A、816O2和818O2互为同位素,性质相似 |
| B、“雨后彩虹”是与胶体、光学等知识有关的自然现象 |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
| D、键角:H2O>C2H2 |





 (R为烃基)
(R为烃基) 反应合成聚碳酯的化学方程式
反应合成聚碳酯的化学方程式