题目内容
下列离子方程式正确的是( )
| A、在硫酸亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | ||||
B、MnO2与浓盐酸反应制取Cl2:MnO2+4HCl(浓)
| ||||
| C、过量的KHSO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | ||||
| D、向稀氢氧化钠溶液中通入少量CO2:OH-+CO2═HCO3- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.亚铁离子被稀硝酸氧化成铁离子,同时生成一氧化氮气体;
B.浓盐酸参加的反应中,浓盐酸需要拆开,不能写成分子形式;
C.硫酸氢钾过量,离子方程式按照氢氧化钡的组成书写;
D.二氧化碳少量,反应生成碳酸钠,不是 碳酸氢钠.
B.浓盐酸参加的反应中,浓盐酸需要拆开,不能写成分子形式;
C.硫酸氢钾过量,离子方程式按照氢氧化钡的组成书写;
D.二氧化碳少量,反应生成碳酸钠,不是 碳酸氢钠.
解答:
解:A.硫酸亚铁溶液中加入稀硝酸,亚铁离子被氧化成铁离子,反应的离子方程式为:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,故A正确;
B.MnO2与浓盐酸反应制取Cl2,浓盐酸应该拆开,正确的离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故B错误;
C.过量的KHSO4与Ba(OH)2溶液反应生成硫酸钡和水,离子方程式按照氢氧化钡的组成书写,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.稀氢氧化钠溶液中通入少量CO2,反应生成碳酸氢钠,正确的离子方程式为:2OH-+CO2═CO32-+H2O,故D错误;
故选A.
B.MnO2与浓盐酸反应制取Cl2,浓盐酸应该拆开,正确的离子方程式为:MnO2+4H++2Cl-
| ||
C.过量的KHSO4与Ba(OH)2溶液反应生成硫酸钡和水,离子方程式按照氢氧化钡的组成书写,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.稀氢氧化钠溶液中通入少量CO2,反应生成碳酸氢钠,正确的离子方程式为:2OH-+CO2═CO32-+H2O,故D错误;
故选A.
点评:本题考查了离子方程式的正误判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等,选项C为易错点,注意反应物过量情况.

练习册系列答案
相关题目
常温下,下列溶液中离子浓度关系表达正确的是( )
| A、Na2CO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) |
| B、0.1mol?L-1的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| C、向NH4HSO4的水溶液中逐滴滴入NaOH溶液,至中性的溶液中:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-) |
| D、pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
有关化学用语正确的是( )
A、-CH3(甲基)的电子式为 |
B、硝基苯的结构简式 |
| C、乙烯的结构简式CH2CH2 |
| D、乙酸的分子式C2H4O2 |
下列反应的离子方程式书写正确的是( )
| A、硫酸铝溶液中加入过量氨水 Al3++30H-═Al(OH)3↓ |
| B、NaHCO3溶液与过量的Ca(OH)2溶液反应 HCO3-+0H-+Ca2+═CaCO3↓+H2O |
| C、碳酸钙与醋酸反应 CaCO3+2H+═Ca2++CO2↑+H2O |
| D、FeI2溶液通入少量Cl2 2Fe2++Cl2═2Fe3++2Cl- |
下列有关阿伏伽德罗常数说法正确的是( )
| A、含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA |
| B、标况下,22.4L四氯化碳所含分子数大于NA |
| C、0.1mol/L的AgNO3溶液中,阳离子所带正电荷数目为0.1NA |
| D、0.2mol/L的H2SO4的硫酸溶液与0.1mol/L的H2SO4的硫酸溶液等质量混合溶液浓度大于0.15mol/L |
下列说法正确的是( )
| A、蛋白质和油脂都属于高分子化合物,一定条件下能水解 |
| B、分子式为C5H12O且氧化产物能发生银镜反应的醇有6种 |
C、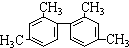 分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面 |
D、1mol β-紫罗兰酮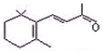 与1mol H2发生加成反应可得到3种不同产物 与1mol H2发生加成反应可得到3种不同产物 |
 ,芳香烃A能发生如图一系列转化:
,芳香烃A能发生如图一系列转化: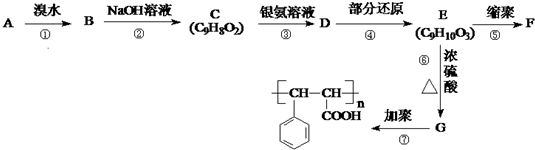
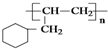 的线路.(用A→…→目标产物 在箭号上写明反应试剂及反应条件.)
的线路.(用A→…→目标产物 在箭号上写明反应试剂及反应条件.)