题目内容
化学与生产、生活和社会密切相关,下列说法正确的是( )
| A、汽车排放的尾气和燃煤排放颗粒污染物是形成雾霾的重要因素 |
| B、为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
| C、高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| D、“低碳”生活倡导节能减排,禁止使用化石燃料,减少污水排放 |
考点:常见的生活环境的污染及治理,硅和二氧化硅,常见的食品添加剂的组成、性质和作用
专题:化学应用
分析:A.化石燃料的燃烧导致PM2.5,可产生雾霾;
B.生石灰不具有还原性;
C.光导纤维的主要原料为二氧化硅;
D.倡导低碳生活,减少化石燃料的使用,而不是禁止使用.
B.生石灰不具有还原性;
C.光导纤维的主要原料为二氧化硅;
D.倡导低碳生活,减少化石燃料的使用,而不是禁止使用.
解答:
解:A.化石燃料的燃烧导致PM2.5,是形成雾霾的重要因素,故A正确;
B.生石灰不具有还原性,只能用于干燥剂,故B错误;
C.光导纤维的主要原料为二氧化硅,故C错误;
D.倡导低碳生活,减少化石燃料的使用,而不是禁止使用,应提高利用率,故D错误.
故选A.
B.生石灰不具有还原性,只能用于干燥剂,故B错误;
C.光导纤维的主要原料为二氧化硅,故C错误;
D.倡导低碳生活,减少化石燃料的使用,而不是禁止使用,应提高利用率,故D错误.
故选A.
点评:本题考查物质的性质,综合考查元素化合物性质,为高频考点,把握常见物质的性质及发生的反应、物质的性质与用途等为解答的关键,选项B为易错点,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
常温下,下列溶液中离子浓度关系表达正确的是( )
| A、Na2CO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) |
| B、0.1mol?L-1的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| C、向NH4HSO4的水溶液中逐滴滴入NaOH溶液,至中性的溶液中:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-) |
| D、pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列反应的离子方程式书写正确的是( )
| A、硫酸铝溶液中加入过量氨水 Al3++30H-═Al(OH)3↓ |
| B、NaHCO3溶液与过量的Ca(OH)2溶液反应 HCO3-+0H-+Ca2+═CaCO3↓+H2O |
| C、碳酸钙与醋酸反应 CaCO3+2H+═Ca2++CO2↑+H2O |
| D、FeI2溶液通入少量Cl2 2Fe2++Cl2═2Fe3++2Cl- |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 0.1mol?L-1的氨水中含有的NH3?H2O分子数为0.1NA |
| B、电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA |
| C、标准状况下,2.24L的二氯甲烷中含有的碳氯共价键的数目为0.2NA |
| D、一定条件下,4.6g NO2和N2O4混合气体中含有的N原子数目为0.1NA |
下列有关阿伏伽德罗常数说法正确的是( )
| A、含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA |
| B、标况下,22.4L四氯化碳所含分子数大于NA |
| C、0.1mol/L的AgNO3溶液中,阳离子所带正电荷数目为0.1NA |
| D、0.2mol/L的H2SO4的硫酸溶液与0.1mol/L的H2SO4的硫酸溶液等质量混合溶液浓度大于0.15mol/L |
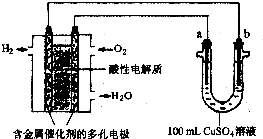 用酸性氢氧燃料电池为电源电解CuSO4溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )
用酸性氢氧燃料电池为电源电解CuSO4溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )| A、燃料电池工作时,负极反应为O2+4H++4e-═2H2O |
| B、a极是石墨,b极是铜时,b极的电极反应为:4OH--4e-═2H2O+O2↑ |
| C、a极是石墨,b极是纯铜时,电解一定时间后两极产生的气体体积都为224ml(标准状况),则原溶液的浓度是0.1mol/L |
| D、a、b两极均是石墨时,若a极产生的气体为56mL(标准状况),则U形管中溶液的PH为2(体积变化忽略不计) |
下列有关化学用语的使用正确的是( )
A、HCl的电子式: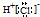 |
B、Cl的原子结构示意图: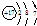 |
| C、乙酸的结构简式:C2H4O2 |
| D、Na2SO4的电离方程式:Na2SO4═Na++SO42- |
下列各醇中,既能发生消去反应又能发生催化氧化反应的是( )
| A、CH3-OH |
B、 |
C、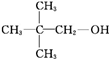 |
D、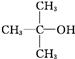 |
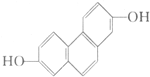 质子核磁共振谱是研究有机化合物结构的有力手段之一.结构中的等效氢原子核磁共振谱中都给出了相应的峰值 (信号),谱中峰的强度与结构中的H原子数成正比.试回答,结构简式为如图所示的有机化合物:
质子核磁共振谱是研究有机化合物结构的有力手段之一.结构中的等效氢原子核磁共振谱中都给出了相应的峰值 (信号),谱中峰的强度与结构中的H原子数成正比.试回答,结构简式为如图所示的有机化合物: