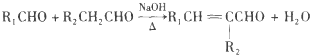题目内容
有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )
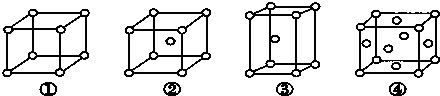

| A、①为简单立方堆积 ②为六方最密堆积 ③为体心立方堆积 ④为面心立方最密堆积 |
| B、晶胞中原子的配位数分别为:①6,②8,③8,④12 |
| C、金属镁采取③的堆积方式 |
| D、空间利用率的大小关系为:①<②<③<④ |
考点:金属晶体的基本堆积模型
专题:化学键与晶体结构
分析:A.②为体心立方堆积,③为六方最密堆积;
B.③为六方密集堆积,配位数为12,不是8;
C.金属镁为六方最密堆积,堆积方式为③;
D.空间利用率中,简单六方堆积的空间利用率最低,空间利用率最高的是③六方最密堆积和④面心立方最密堆积.
B.③为六方密集堆积,配位数为12,不是8;
C.金属镁为六方最密堆积,堆积方式为③;
D.空间利用率中,简单六方堆积的空间利用率最低,空间利用率最高的是③六方最密堆积和④面心立方最密堆积.
解答:
解:A.②是体心立方堆积,属于钾、钠和铁型,③是六方最密堆积,属于镁、锌、钛型,故A错误;
B.③为六方最密堆积,③的配位数是12,所以晶胞中原子的配位数分别为:①6,②8,③12,④12,故B错误;
C.镁的堆积方式为六方最密堆积,所以金属镁采取③的堆积方式,故C正确;
D.①中空间利用率为51%,②中空间利用率为68%,③④中空间利用率为74%,所以空间利用率大小关系为:①<②<③=④,故D错误;
故选C.
B.③为六方最密堆积,③的配位数是12,所以晶胞中原子的配位数分别为:①6,②8,③12,④12,故B错误;
C.镁的堆积方式为六方最密堆积,所以金属镁采取③的堆积方式,故C正确;
D.①中空间利用率为51%,②中空间利用率为68%,③④中空间利用率为74%,所以空间利用率大小关系为:①<②<③=④,故D错误;
故选C.
点评:本题考查了金属晶体结构,题目难度中等,注意掌握典型晶体晶胞结构,明确晶胞中配位数、原子个数的计算方法,为学习的难点.

练习册系列答案
相关题目
常温下,下列溶液中离子浓度关系表达正确的是( )
| A、Na2CO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) |
| B、0.1mol?L-1的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| C、向NH4HSO4的水溶液中逐滴滴入NaOH溶液,至中性的溶液中:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-) |
| D、pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
如图是电解溶液CuCl2的装置,其中c、d为石墨电极,则下列有关判断正确的是( )


| A、a为正极、d为阴极 |
| B、c电极发生还原反应 |
| C、电解过程中,d电极质量增加 |
| D、电解过程中,氯离子浓度不变 |
下列反应的离子方程式书写正确的是( )
| A、硫酸铝溶液中加入过量氨水 Al3++30H-═Al(OH)3↓ |
| B、NaHCO3溶液与过量的Ca(OH)2溶液反应 HCO3-+0H-+Ca2+═CaCO3↓+H2O |
| C、碳酸钙与醋酸反应 CaCO3+2H+═Ca2++CO2↑+H2O |
| D、FeI2溶液通入少量Cl2 2Fe2++Cl2═2Fe3++2Cl- |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 0.1mol?L-1的氨水中含有的NH3?H2O分子数为0.1NA |
| B、电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA |
| C、标准状况下,2.24L的二氯甲烷中含有的碳氯共价键的数目为0.2NA |
| D、一定条件下,4.6g NO2和N2O4混合气体中含有的N原子数目为0.1NA |
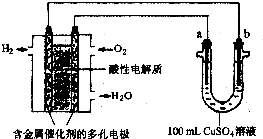 用酸性氢氧燃料电池为电源电解CuSO4溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )
用酸性氢氧燃料电池为电源电解CuSO4溶液,实验装置如图所示.下列关于此装置的说法中,正确的是( )| A、燃料电池工作时,负极反应为O2+4H++4e-═2H2O |
| B、a极是石墨,b极是铜时,b极的电极反应为:4OH--4e-═2H2O+O2↑ |
| C、a极是石墨,b极是纯铜时,电解一定时间后两极产生的气体体积都为224ml(标准状况),则原溶液的浓度是0.1mol/L |
| D、a、b两极均是石墨时,若a极产生的气体为56mL(标准状况),则U形管中溶液的PH为2(体积变化忽略不计) |
如图为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述中不正确的是( )
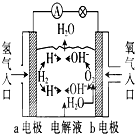

| A、a电极是负极 |
| B、b电极的电极反应式为4OH--4e-═2H2O+O2↑ |
| C、在电池内部,H+向b电极附近运动 |
| D、氢氧燃料电池是一种具有广泛应用前景的绿色电源 |
 糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志.长期摄入高热量食品和缺少运动都易导致糖尿病.
糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志.长期摄入高热量食品和缺少运动都易导致糖尿病.

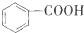 (-R1、-R2表示氢原子或烃基);
(-R1、-R2表示氢原子或烃基);