题目内容
9.下列关于浓硫酸和浓硝酸的叙述错误的是( )| A. | 常温下都能与铜较快反应 | |
| B. | 和铜反应中都表现出强氧化性和强酸性 | |
| C. | 都可以储存于铝制槽罐中 | |
| D. | 分别露置在空气中,容器内溶质的物质的量浓度都降低 |
分析 A、铜和浓硫酸的反应需加热;
B、浓硫酸、浓硝酸和铜反应均生成铜盐和NO2、SO2;
C、浓硫酸和浓硝酸均能使铝钝化;
D、浓硫酸易吸水,浓硝酸易挥发.
解答 解:A、铜和浓硫酸的反应需加热,在常温下铜和浓硫酸不反应,故A错误;
B、浓硫酸、浓硝酸和铜反应均生成铜盐和NO2、SO2,生成盐的硫酸和硝酸做酸,生成NO2、SO2的硝酸、硫酸做强氧化剂,故B正确;
C、浓硫酸和浓硝酸均能使铝钝化,故浓硫酸和浓硝酸可以用铝制槽罐来储存,故C正确;
D、浓硫酸易吸水,故浓硫酸露置在空气中后溶液体积增大,则浓度减小;浓硝酸易挥发,露置在空气中后硝酸挥发导致浓度减小,故D正确.
故选A.
点评 本题考查了浓硫酸和浓硝酸的性质,掌握物质的性质是解题关键,难度不大.

练习册系列答案
相关题目
11.下列方程式书写正确的是( )
| A. | H2S的电离方程式:H2S+H2O?H3O++HS- | |
| B. | NaHCO3在水溶液中的电离方程式:NaHCO3=Na++H++CO32- | |
| C. | CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- | |
| D. | HS-的水解方程式:HS-+H2O?S2-+H3O+ |
20.在无色透明的酸性溶液中,下列离子能大量共存的是( )
| A. | K+、Cu2+、NO3-、SO42- | B. | CO32-、Na-、Cl-、SO42- | ||
| C. | Al3+、Cl-、NO3-、Mg2+ | D. | H+、Ba2+、NO3-、SO42- |
17.关于共价键,下列说法不正确的是( )
| A. | 按共用电子对是否偏移,可以把共价键划分为极性键和非极性键 | |
| B. | 按原子轨道的重叠方式,分为σ键和π 键 | |
| C. | 按共用电子对的提供方式,分为配位键和普通共价键 | |
| D. | 所有分子中都含有共价键 |
4.实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置蒸发皿;②放置酒精灯;③固定铁圈位置;④停止加热,余热蒸干;⑤加热搅拌.其正确的操作顺序为( )
| A. | ②③④⑤① | B. | ①②③④⑤ | C. | ②③①⑤④ | D. | ②①③④⑤ |
14.下列依据相关实验得出的结论正确的是( )
| A. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| B. | 将Fe(NO3)2样品溶于稀盐酸中,然后滴加KSCN溶液,溶液变红,说明Fe(NO3)2样品已氧化变质 | |
| C. | 在食盐试样中加入盐酸和KI溶液,加入淀粉溶液后变蓝,说明食盐试样中可能含有KIO3 | |
| D. | 加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在 |
1.在盛放浓硫酸的试剂瓶上应印有如图所示警示标记中的( )
| A. |  | B. |  | C. |  | D. | 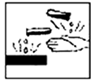 |
18.NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1molCl2溶于足量水中,转移的电子数为0.1NA | |
| B. | 100g98%的浓硫酸中,氧原子总数为4NA | |
| C. | 常温常压下,3g甲醛所含σ键数目为0.3NA | |
| D. | 1molFeCl3与沸水反应生成胶体后,含有的Fe(OH)3胶粒数目为NA |
4.某同学体检的血液化验单中,葡萄糖为0.0059mol•L?1.表示该体检指标的物理量是( )
| A. | 溶解度(S) | B. | 物质的量浓度(c) | C. | 质量分数(ω) | D. | 摩尔质量(M) |