题目内容
11.下列方程式书写正确的是( )| A. | H2S的电离方程式:H2S+H2O?H3O++HS- | |
| B. | NaHCO3在水溶液中的电离方程式:NaHCO3=Na++H++CO32- | |
| C. | CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- | |
| D. | HS-的水解方程式:HS-+H2O?S2-+H3O+ |
分析 A、多元弱酸的电离分步进行,且用可逆号;
B、碳酸氢钠在溶液中只能完全电离为钠离子和碳酸氢根离子;
C、多元弱酸根的水解分步进行,且进行不彻底;
D、HS-水解为H2S.
解答 解:A、多元弱酸的电离分步进行,且用可逆号,故H2S的电离方程式为:H2S+H2O?H3O++HS-,故A正确;
B、碳酸氢钠在溶液中只能完全电离为钠离子和碳酸氢根离子,故NaHCO3在水溶液中的电离方程式:NaHCO3=Na++HCO3-,故B错误;
C、多元弱酸根的水解分步进行,且进行不彻底,故CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,故C错误;
D、HS-水解为H2S,故水解方程式为:HS-+H2O?H2S+OH-,故D错误.
故选A.
点评 本题考查了电离方程式和水解方程式的区别,应注意的是HS-和HCO3-等酸式弱酸根的电离方程式和水解方程式的区别.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
1.下列物质的用途是应用其化学性质的是( )
| A. | 用铁罐储存浓硝酸 | |
| B. | 用MgO、Al2O3制作耐高温坩埚 | |
| C. | 用铁芯铝绞线作为高压输电线材料 | |
| D. | 用钠钾合金作为快中子反应堆的热交换剂 |
19.对于下列两个转化关系,说法不正确的是( )
(1)FeS2$\stackrel{①}{→}$SO2$\stackrel{②}{→}$SO3$\stackrel{③}{→}$H2SO4
(2)N2$\stackrel{④}{→}$NO$\stackrel{⑤}{→}$NO2$\stackrel{⑥}{→}$HNO3$\stackrel{⑦}{→}$KNO3.
(1)FeS2$\stackrel{①}{→}$SO2$\stackrel{②}{→}$SO3$\stackrel{③}{→}$H2SO4
(2)N2$\stackrel{④}{→}$NO$\stackrel{⑤}{→}$NO2$\stackrel{⑥}{→}$HNO3$\stackrel{⑦}{→}$KNO3.
| A. | (1)符合工业接触法制硫酸的流程 | |
| B. | (2)反映出“雷雨发庄稼”的实质 | |
| C. | 反应②的条件为“催化剂、加热”,属于不可逆反应 | |
| D. | 反应④属于“氮的固定” |
6.下列说法正确的是( )
| A. | Na2CO3溶液 c(Na+ )与 c(CO3)之比为 2:1 | |
| B. | pH=2 和 pH=1 的硝酸中 c(H+)之比为 1:2 | |
| C. | 0.2mol/L 与 0.1mol/L 醋酸中 c(H+)之比为 2:1 | |
| D. | pH=1 的硫酸中加入等体积 0.1mol/L 的 NaOH 溶液,两者恰好完全反应 |
16.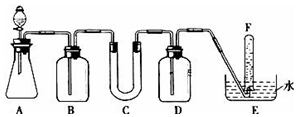 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
(1)填写表中空格:
已知A中放有碳酸钙,分液漏斗装稀盐酸
(2)为了达到实验目的,不需要(填“需要”或“不需要”)在B装置之后增加一个吸收水蒸气的装置;
(3)试管F中收集满气体后,下一步实验操作是:把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,立即用带火星的木条伸到试管F的管口,如果木条复燃,说明过氧化钠与二氧化碳反应产生氧气,可做供氧剂.
 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品.用图中的实验装置进行实验,证明过氧化钠可作供氧剂.(1)填写表中空格:
已知A中放有碳酸钙,分液漏斗装稀盐酸
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2气体中混入的HCl |
| C | 石棉绒与过氧化钠 | 与CO2反应,产生O2 |
| D | NaOH溶液 | 吸收未反应的CO2气体 |
(3)试管F中收集满气体后,下一步实验操作是:把E中的导管移出水面,关闭分液漏斗的活塞,用拇指堵住试管口,取出试管,立即用带火星的木条伸到试管F的管口,如果木条复燃,说明过氧化钠与二氧化碳反应产生氧气,可做供氧剂.
3.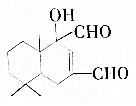 科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如图.下列关于化合物A的说法正确的是( )
科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如图.下列关于化合物A的说法正确的是( )
 科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如图.下列关于化合物A的说法正确的是( )
科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种,其结构如图.下列关于化合物A的说法正确的是( )| A. | 化合物A的分子式为C15H22O3 | |
| B. | 与FeCl3溶液发生反应后溶液显紫色 | |
| C. | 1molA最多能与2mol新制的Cu(OH)2悬浊液反应 | |
| D. | 1molA最多能与1molH2发生加成反应 |
8.在下列实验操作中错误的是( )
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计的水银球靠近蒸馏烧瓶的瓶底 | |
| C. | 过滤时,玻璃棒在引流过程中应放在三层滤纸处 | |
| D. | 称量时,称量物置于托盘天平左盘,砝码放在托盘天平右盘 |
9.下列关于浓硫酸和浓硝酸的叙述错误的是( )
| A. | 常温下都能与铜较快反应 | |
| B. | 和铜反应中都表现出强氧化性和强酸性 | |
| C. | 都可以储存于铝制槽罐中 | |
| D. | 分别露置在空气中,容器内溶质的物质的量浓度都降低 |



