题目内容
 面对全球近期的气候异常,环境问题再次成为焦点.怎样消除现有大气污染,开发利用新能源,是目前化学研究的一个重要方向.
面对全球近期的气候异常,环境问题再次成为焦点.怎样消除现有大气污染,开发利用新能源,是目前化学研究的一个重要方向.(1)汽车尾气治理的方法之一是在汽车的排气管上安装一个“催化转化器”.
已知反应2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-113kJ/mol
①实验发现该反应在100℃~400℃的温度范围内,温度每升高10℃,反应速率却约为原来的3倍,在400℃~450℃时,温度每升高10℃,反应速率却约为原来的10倍,而温度高于450℃时,温度每升高10℃,反应速率又约为原来的3倍.若其他反应条件不变,试分析造成这种现象的可能原因是
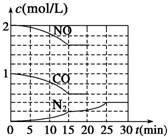
②为了模拟催化转化器的工作原理,在T℃时,将2mol NO与1mol CO充入1L反应容器中,反应过程中NO(g)、CO(g)、N2(g)的物质的量浓度变化如右图所示,则反应进行到15min时,NO的平均反应速率为
③写出该反应的化学平衡常数表达式K=
当25min达到平衡后,若保持体系温度、容积不变,再向容器中充入NO、N2气体各1mol,平衡将
(2)将固态能源转化为气态、液体能源是能源研究的重点之一.
已知:C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ/molⅠ
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/molⅡ
2H2(g)+O2(g)═2H2O(g)△H=-484kJ/molⅢ
试写出由C与水蒸气在高温条件下反应生成氢气和一氧化碳的热化学方程式:
(3)燃料电池的研究和发展也是目前的研究重点.如用氢氧化钾溶液作电解质溶液,用多孔石墨作电极,在电极上分别充入乙烷和氧气.写出负极的电极反应式:
考点:化学反应速率的影响因素,用盖斯定律进行有关反应热的计算,原电池和电解池的工作原理,反应速率的定量表示方法,化学平衡的影响因素
专题:
分析:(1)①根据催化剂的活性受温度影响;
②根据V=
来计算;
③化学平衡常数等于平衡时生成物的浓度幂之积比上反应物浓度幂之积;先根据三段法求出各自的浓度,然后求出平衡常数和浓度熵,最后根据平衡常数的大小与浓度熵的大小来确定平衡移动方向;平衡常数是温度的函数,温度不变平衡常数不变;
(2)根据盖斯定律进行解答;
(3)根据原电池中负极失电子,发生氧化反应;正极上得到电子,发生还原反应;分析电极反应,根据电子守恒结合总反应和正极反应计算得到负极电极反应.
②根据V=
| ||
| △t |
③化学平衡常数等于平衡时生成物的浓度幂之积比上反应物浓度幂之积;先根据三段法求出各自的浓度,然后求出平衡常数和浓度熵,最后根据平衡常数的大小与浓度熵的大小来确定平衡移动方向;平衡常数是温度的函数,温度不变平衡常数不变;
(2)根据盖斯定律进行解答;
(3)根据原电池中负极失电子,发生氧化反应;正极上得到电子,发生还原反应;分析电极反应,根据电子守恒结合总反应和正极反应计算得到负极电极反应.
解答:
解:①因催化剂的活性受温度影响,由信息可知催化剂在400℃~450℃活性最大,故答案为:催化剂在400℃~450℃活性最大;
②由图象可知在15min内NO的物质的量变化0.4mol,则NO的平均反应速率为=
mol?L-1?min-1=0.027 mol?L-1?min-1,故答案为:0.027 mol?L-1?min-1;
③化学平衡常数等于平衡时生成物的浓度幂之积比上反应物浓度幂之积,所以K=
,由平衡常数表达式可知一氧化氮的系数是2次方,所以再向容器中充入NO、N2气体各1mol,分母增加的幅度大,导致QC减小,所以平衡逆向移动,即向左移动,而温度不变,所以K值不变,
故答案为:
;向左;不变;
(2)C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ/mol;A
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol;B
2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol;C
将ABC三式作如下变换,A-
C-
B可得:C(S)+H2O(g)
CO(g)+H2(g) △H=+131KJ/mol,故答案为:C(S)+H2O(g)
CO(g)+H2(g) △H=+131KJ/mol;
(3)①2 C2H6+7 O2→4 CO2+6 H2O,设计原电池,根据化合价变化分析判断,乙烷失电子发生氧化反应,所以通入乙烷气体的电极应为负极,正极电极反应为:②O2+2H2O+4e-=4OH-;①-②×7得到负极电极反应为:C2H6-14e-+18OH-═2CO32-+12H2O;
故答案为:C2H6-14e-+18OH-═2CO32-+12H2O.
②由图象可知在15min内NO的物质的量变化0.4mol,则NO的平均反应速率为=
| ||
| 15 |
③化学平衡常数等于平衡时生成物的浓度幂之积比上反应物浓度幂之积,所以K=
| c(N2)?c2(CO2) |
| c2(NO)?c2(CO) |
故答案为:
| c(N2)?c2(CO2) |
| c2(NO)?c2(CO) |
(2)C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ/mol;A
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol;B
2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol;C
将ABC三式作如下变换,A-
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| ||
(3)①2 C2H6+7 O2→4 CO2+6 H2O,设计原电池,根据化合价变化分析判断,乙烷失电子发生氧化反应,所以通入乙烷气体的电极应为负极,正极电极反应为:②O2+2H2O+4e-=4OH-;①-②×7得到负极电极反应为:C2H6-14e-+18OH-═2CO32-+12H2O;
故答案为:C2H6-14e-+18OH-═2CO32-+12H2O.
点评:本题考查了热化学方程式的书写、燃料电池电极反应式的书写、化学反应速率和化学平衡移动的相关知识,题目难度中等,明确电解池工作原理是解题关键.

练习册系列答案
相关题目
下列说法正确的是( )
| A、脱脂棉的主要成分是纤维素,人造丝和蚕丝的主要成分都是蛋白质 |
| B、淀粉、油脂、蛋白质都是高分子化合物,在一定条件下都能发生水解 |
| C、肽链通过氢键按一定的规律卷曲或折叠形成的空间结构称为蛋白质的二级结构 |
| D、淀粉与稀硫酸混合加热后,加入新制氢氧化铜加热,可检验淀粉是否已水解 |
浓度为0.1mol/L的(NH4)2SO4溶液中各种离子浓度的大小顺序正确的是( )
| A、C(SO42-)>C(NH4+)>C(OH-)>C(H+) |
| B、C(NH4+)>C(SO42-)>C(H+)>C(OH-) |
| C、C(SO42-)>C(NH4+)>C(H+)>C(OH-) |
| D、C(SO42-)>C(H+)>C(NH4+)>C(OH-) |
t℃时,水的离子积为KW.在该温度下、混合可溶性的一元酸HA和一元碱BOH的溶液,下列有关混合液的各种
关系中,可确认混合液呈中性的是( )
关系中,可确认混合液呈中性的是( )
A、[OH-]=
| ||
| B、[A-]>[B+] | ||
| C、pH=7 | ||
| D、[H+]-[OH-]=[A-]-[B+] |
下列命名正确的是( )
| A、2,4,4-三甲基戊烷 |
| B、4-甲基-2-乙基辛烷 |
| C、2-甲基-1,3-丁二烯 |
| D、2-甲基-1-丙烯 |
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
| A、分别加热这两种固体物质,并将生成的气体通入澄清石灰水中 |
| B、分别在这两种物质的溶液中,加入Ca(NO3)2溶液 |
| C、分别在这两种物质的溶液中,加入少量澄清石灰水 |
| D、分别在这两种固体溶液中,加入同浓度的稀盐酸 |
化学知识在工农业生产和日常生活中有着重要的应用.下列说法正确的是( )
| A、Na2O2、H2O2所含化学键完全相同,都能做供氧剂 |
| B、糖类、蛋白质、油脂、PVC都属于天然高分子化合物 |
| C、常温下,浓硫酸、浓硝酸与铁均能发生钝化,均能用铁罐储运 |
| D、制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |



