题目内容
2.亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌.如图1是制取来氯酸钠的工艺流程: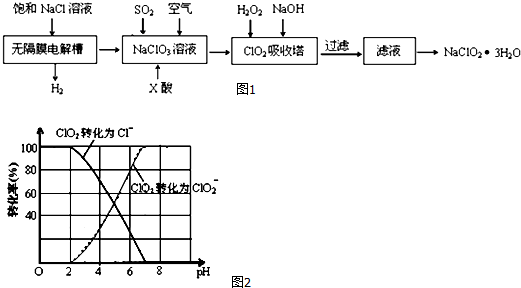
已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用.②ClO2气体在中性和碱性溶液中不能稳定存在.
(1)反应生成ClO2气体需要X酸酸化,X酸可以为B.
A.盐酸 B.稀硫酸 C.硝酸 D.H2C2O4溶液
(2)吸收塔内的温度不能过高的原因为温度过高H2O2将分解.
(3)ClO2被S ClO2被S2-还原为ClO2-、Cl-转化率与pH关系如图2所示.写出pH≤2时ClO2与S2- 反应的离子方程式:2ClO2+5S2-+8H+=2Cl-+5S↓+4H2O.
分析 无隔膜电解槽中持续电解饱和氯化钠溶液,则电解生成的氯气和氢氧化钠反应生成氯酸钠溶液,通二氧化硫和X酸还原氯酸钠溶液生成二氧化氯,再用双氧水、氢氧化钠吸收反应生成亚氯酸钠,过滤的亚氯酸钠(NaClO2)溶液通过蒸发结晶得到亚氯酸钠晶体,以此解答;
(1)由于ClO2气体在中性和碱性溶液中不能稳定存在,所以只能在酸性环境中存在.由于在酸性条件下,氯酸钠容易和盐酸发生氧化还原反应,所以X应该是硫酸;
(2)H2O2不稳定,温度过高,H2O2容易分解,吸收塔的温度不能过高,其目的是防止H2O2分解;
(3)根据图象可知,pH≤2时ClO2被还原为Cl-,所以该反应的离子方程式是2ClO2+5S2-+8H+=2Cl-+5S↓+4H2O.
解答 解:(1)由于ClO2气体在中性和碱性溶液中不能稳定存在,所以只能在酸性环境中存在.由于在酸性条件下,氯酸钠容易和盐酸发生氧化还原反应,所以X应该是硫酸,故答选:B;
(2)H2O2不稳定,温度过高,H2O2容易分解,吸收塔的温度不能过高,其目的是防止H2O2分解,故答案为:温度过高H2O2将分解;
(3)根据图象可知,pH≤2时ClO2被还原为Cl-,所以该反应的离子方程式是2ClO2+5S2-+8H+=2Cl-+5S↓+4H2O,故答案为:2ClO2+5S2-+8H+=2Cl-+5S↓+4H2O.
点评 本题考查亚氯酸钠的制备,以过氧化氢法制备亚氯酸钠为主线,考查学生阅读题目获取信息的能力、对浓度概念的理解、对氧化还原反应相关知识的运用、有关实验操作和简单实验设计能力考察以及在新情境下综合运用知识解决问题的能力,题目难度中等.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
17.不能用H++OH-=H2O表示的反应是( )
| A. | 盐酸与氢氧化钾溶液反应 | B. | 稀盐酸与氢氧化钠溶液反应 | ||
| C. | 稀硝酸与氢氧化钠溶液反应 | D. | 硅酸与氢氧化钠溶液反应 |
13.下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A. | 都具有吸水性 | |
| B. | 露置于空气中都能形成白雾 | |
| C. | 露置于空气中,溶液浓度均降低 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
10.下列实验基本操作及注意事项中,主要出于安全考虑的是( )
| A. | 实验剩余的药品不能放回原试剂瓶 | |
| B. | 酒精灯内酒精不能多于酒精灯容积的2/3 | |
| C. | 实验结束后将试管清洗干净 | |
| D. | 胶头滴管不能交叉使用 |
17.下列描述正确的是( )
| A. | 氯水的标签上应标注: | B. | O2-的结构示意图: | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | BeCl2的电子式: |
14.实验室常用NH4Cl和NaNO2反应制取N2.下列有关说法正确的是( )
| A. | NH4Cl中N元素被还原 | |
| B. | NaNO2是还原剂 | |
| C. | 生成1 mol N2时转移6 mol电子 | |
| D. | 氧化剂和还原剂的物质的量之比是1:1 |
11.遇有下列情况,处理不当的是( )
| A. | 不小心将少量浓硫酸沾到皮肤上,立即用水冲洗 | |
| B. | 皮肤上沾有苯酚时,立即用酒精擦洗 | |
| C. | 误食重金属盐,立即喝生牛奶或蛋清 | |
| D. | 金属钠着火,立刻用砂子盖灭 |
