题目内容
煤的气化的液化不仅可以使煤变成清洁的能源,也是化工原料的重要来源之一,下图是由煤气化后的产物进行化学合成的一系列转化,其中,F分子中的碳原子数是E的3倍;E分子中含有两个相同的官能团,且两个官能团不边顺同一个碳原子上;M分子中含有4个碳原子。其它与本题无关的生物均已略去。

请回答下列问题:
(1)写出下列物质的结构简式并回答问题:
A为___________;D为___________;A与H两物质相互关系是___________。
(2)写出下列反应的化学方程式并指出E→F的反应类型:CH2COOH+E→F__________反应类型____________;M与新制的氢氧化铜悬浊液共热_______。
(3)与H互为同分异构体且与H含有相同官能团,但在碳链不变的情况下不能催化氧化的化合物结构简式为______________。
(1)CH3OH CHO
HOCH2CHO(答为 CHO、HOCH=CHOH等合理的结构也给分)
同系物
(2)2CH3COOH+HOCH2CH2OH ![]() CH3COOOCH2CH2OOCCH3+2H2O
CH3COOOCH2CH2OOCCH3+2H2O
酯化反应
CH3CH2CH2CHO+2Cu(OH)2 ![]() CH3CH2CH2COOH+Cu2O↓+2H2O
CH3CH2CH2COOH+Cu2O↓+2H2O
(3)C(CH3)3OH (其他合理的书写形式参照给分)

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
下列说法中不正确的是( )
| A、与煤油、柴油相比较,天然气是一种比较清洁的化石燃料 | B、乙醇是一种可再生能源,作为燃料的优点的是完全燃烧的产物不污染环境 | C、利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量 | D、煤的气化和液化不仅可以获得洁净燃料,而且再燃烧会放出更多的热量 |
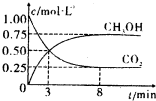 (2012?枣庄二模)碳和碳的化合物在人类生产、生活中的应用非常广泛,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
(2012?枣庄二模)碳和碳的化合物在人类生产、生活中的应用非常广泛,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视. =a,则a的取值范围为______.
=a,则a的取值范围为______.