题目内容
下列计算或推导结果正确的是( )
| A、10.8 g X2O5中含有0.5 mol O,则X的相对原子质量为28 |
| B、4 g某气体含有的分子数为3.01×1023,则2 g该气体在标准状况下的体积是5.6 L |
| C、同温同压下,10 L X2气体跟30 L Y2气体化合生成20 L某Z气体,则Z的化学式为XY2 |
| D、标准状况下,相同质量的N2、O2、Cl2中,体积最大的是Cl2 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.根据分子构成结合M=
计算;
B.根据n=
=
=
计算;
C.在一定温度和压强下,气体的体积与物质的量成正比,化学反应遵循质量守恒定律,根据质量守恒解答;
D.根据n=
=
计算.
| m |
| n |
B.根据n=
| m |
| M |
| N |
| NA |
| V |
| Vm |
C.在一定温度和压强下,气体的体积与物质的量成正比,化学反应遵循质量守恒定律,根据质量守恒解答;
D.根据n=
| m |
| M |
| V |
| Vm |
解答:
解:A.X2O5中含有0.5 mol O,则n(X2O5)=0.1mol,M(X2O5)=
=108g/mol,X的相对原子质量为
=14,故A错误;
B.4 g气体分子数为3.01×1023,物质的量为0.5mol,则2 g该气体的物质的量为0.25mol,该气体在标准状况下的体积是0.25mol×22.4L/mol=5.6 L,故B正确;
C.在一定温度和压强下,气体的体积与物质的量成正比,
设X2的物质的量为10mol,则Y2的物质的量为30mol,Z的物质的量为20mol,
化学反应遵循质量守恒定律,
物质的量之比等于化学计量数之比,
则有X2+3Y2=2Z,
Z的化学式为XY3,
故C错误;
D.M(Cl2)>M(O2)>M(N2),相同质量时N2的物质的量最大,体积最大,故D错误.
故选B.
| 10.8g |
| 0.1mol |
| 108-16×5 |
| 2 |
B.4 g气体分子数为3.01×1023,物质的量为0.5mol,则2 g该气体的物质的量为0.25mol,该气体在标准状况下的体积是0.25mol×22.4L/mol=5.6 L,故B正确;
C.在一定温度和压强下,气体的体积与物质的量成正比,
设X2的物质的量为10mol,则Y2的物质的量为30mol,Z的物质的量为20mol,
化学反应遵循质量守恒定律,
物质的量之比等于化学计量数之比,
则有X2+3Y2=2Z,
Z的化学式为XY3,
故C错误;
D.M(Cl2)>M(O2)>M(N2),相同质量时N2的物质的量最大,体积最大,故D错误.
故选B.
点评:本题综合考查阿伏加德罗定律及推论,为高频考点,侧重于学生的分析能力和计算能力的考查,题目难度不大,注意从质量守恒的角度解答该题,把握相关计算公式的运用.

练习册系列答案
 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
最简式相同,但既不是同系物又不是同分异构体的是( )
A、CH≡CH和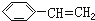 |
| B、甲醚和甲醇 |
| C、环丙烷和环己烷 |
D、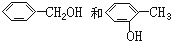 |
相同体积的Na2SO4溶液(浓度为c1)和Al2(SO4)3溶液(浓度为c2),若其中SO42-的物质的量浓度相同,则c1和c2的关系是( )
| A、c1=c2 |
| B、c1=3 c2 |
| C、c2=3 c1 |
| D、无法确定 |
设NA是阿伏加德罗常数的数值,下列说法不正确的是( )
| A、1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| B、标准状况下,2.24 L Cl2溶于水,转移的电子数目为0.1NA |
| C、常温常压下,8 g SO3所含的氧原子的数目为0.3NA |
| D、过氧化钠与H2O反应,每生成0.1mol氧气,转移电子的数目为0.2NA |
下列说法中正确的是( )
| A、固体NaCl不导电,但NaCl是电解质 |
| B、Cu能导电,所以Cu是电解质 |
| C、NH3溶于水能导电,所以NH3是电解质 |
| D、BaSO4的水溶液不导电,所以BaSO4是非电解质 |
下列现象中,不能用胶体知识解释的是( )
| A、向豆浆中加入盐卤可制作豆腐 |
| B、清晨在密林中看到一缕缕光束 |
| C、在河水与海水的交汇处,有沙洲形成 |
| D、向FeCl3溶液中加入Na2CO3溶液,会出现红褐色沉淀 |