题目内容
在1大气压、120℃时的某密闭容器中充满H2S和O2的混合气体,用电火花点燃,充分反应后,恢复到120℃时,测得容器内气体压强为0.75大气压.试求原混合气体中H2S和O2的体积之比.
考点:阿伏加德罗定律及推论,化学方程式的有关计算
专题:计算题
分析:H2S和O2反应方程式为2H2S+O2
2S+2H2O,温度和容器体积不变,则容器内气体压强之比等于其物质的量之比,反应前后气体压强之比为1:0.75=4:3,则反应前后气体的物质的量之比为4:3,相同条件下,气体体积之比等于其物质的量之比,再根据硫化氢和氧气之间的关系式确定二者体积之比.
| ||
解答:
解:H2S和O2反应方程式为2H2S+O2
2S+2H2O,温度和容器体积不变,则容器内气体压强之比等于其物质的量之比,反应前后气体压强之比为1:0.75=4:3,则反应前后气体的物质的量之比为4:3,相同条件下,气体体积之比等于其物质的量之比,
(1)当H2S过量时,氧气不足量,反应前后气体的物质的量之比为4:3,设反应前混合气体的物质的量为4mol,则反应后气体的物质的量为3mol,气体的物质的量减少1mol,设氧气的物质的量为x,
2H2S+O2
2S+2H2O 气体的物质的量减少
1mol 1mol
x 1mol
1mol:1mol=x:1mol,所以x=1mol,则硫化氢的物质的量为4mol-1mol=3mol,
相同条件下,气体的物质的量之比等于其体积之比,所以原混合气体中H2S和O2的体积之比=3mol:1mol=3:1;
(2)当O2过量时,则H2S不足量,反应前后气体的物质的量之比为4:3,设反应前混合气体的物质的量为4mol,则反应后气体的物质的量为3mol,气体的物质的量减少1mol,设H2S的物质的量为y,
2H2S+O2
2S+2H2O 气体的物质的量减少
2mol 1mol
y 1mol
2mol:1mol=y:1mol,y=2mol,
则氧气的物质的量=4mol-2mol=2mol,
相同条件下,气体的物质的量之比等于其体积之比,所以原混合气体中H2S和O2的体积之比=2mol:2mol=1:1,
答:原混合气体中H2S和O2的体积之比为3:1或1:1.
| ||
(1)当H2S过量时,氧气不足量,反应前后气体的物质的量之比为4:3,设反应前混合气体的物质的量为4mol,则反应后气体的物质的量为3mol,气体的物质的量减少1mol,设氧气的物质的量为x,
2H2S+O2
| ||
1mol 1mol
x 1mol
1mol:1mol=x:1mol,所以x=1mol,则硫化氢的物质的量为4mol-1mol=3mol,
相同条件下,气体的物质的量之比等于其体积之比,所以原混合气体中H2S和O2的体积之比=3mol:1mol=3:1;
(2)当O2过量时,则H2S不足量,反应前后气体的物质的量之比为4:3,设反应前混合气体的物质的量为4mol,则反应后气体的物质的量为3mol,气体的物质的量减少1mol,设H2S的物质的量为y,
2H2S+O2
| ||
2mol 1mol
y 1mol
2mol:1mol=y:1mol,y=2mol,
则氧气的物质的量=4mol-2mol=2mol,
相同条件下,气体的物质的量之比等于其体积之比,所以原混合气体中H2S和O2的体积之比=2mol:2mol=1:1,
答:原混合气体中H2S和O2的体积之比为3:1或1:1.
点评:本题考查了根据方程式进行计算,根据方程式中各个物理量之间的关系式进行计算,注意要分情况讨论,该温度下水是气体,为易错点.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
下列离子方程式书写正确的是( )
| A、过量的SO2通入NaOH溶液中:SO2+2OH-=SO32-+H2O |
| B、NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3+2H2O+CO32- |
| C、向氯化铝溶液中加过量氨水:Al3++4NH3.H2O=AlO2-+4NH4++2H2O |
| D、FeSO4酸性溶液暴露在空气中:Fe2++O2+4H+=4Fe3++2H2O |
将30mL 0.5mol/L的CuSO4溶液加水稀释到500mL,稀释后的CuSO4物质的量浓度为( )
| A、0.3mol/L |
| B、0.03mol/L |
| C、0.05mol/L |
| D、0.04mol/L |
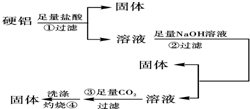 硬铝中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如图所示实验:
硬铝中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如图所示实验:
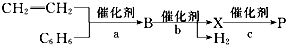
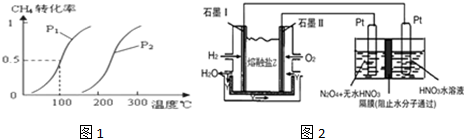

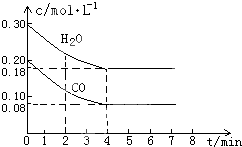 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示反应物的转化率越
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示反应物的转化率越