题目内容
 A、B、C是由元素周期表中前18号元素中的3种元素形成的单质,甲、乙是常见的化合物.它们之间存在如图所示关系.
A、B、C是由元素周期表中前18号元素中的3种元素形成的单质,甲、乙是常见的化合物.它们之间存在如图所示关系.
(1)如图反应①~③中属于化合反应的是______(填序号).化合反应有多种类别,试举出一个与图中化合反应类别不同的实例(用化学方程式表示):______.
(2)若甲常温下呈液态,A常温下是固态非金属单质,则乙的化学式是______.若甲常温下呈液态,A常温下是气态非金属单质,则乙的电子式是______.
(3)若甲常温下呈气态,A是常见的金属单质,写出A和甲在一定条件下反应的化学方程式:______.
(4)若A、B属于同一主族的高硬度单质,则A的同素异形体与甲的反应在工业上的用途是______.
解:(1)化合反应是两种或两种以上的物质生产一种物质的反应,图中①③位化合反应,图中化合反应的反应物都是单质,可为化合物的化合反应,如H2O+CO2=H2CO3,故答案为:①③;H2O+CO2=H2CO3;
(2)若甲常温下呈液态,应为H2O,A常温下是固态非金属单质,应为碳,则乙是CO,B是H2,C是O2;若A常温下是气态非金属单质,应为F2,乙是HF,B是O2,C是H2,乙的电子式为 ,故答案为:CO;
,故答案为:CO; ;
;
(3)若甲常温下呈气态,A是常见的金属单质,应为Mg,甲是CO2;乙是Mg,B是C,C是O2,A和甲在一定条件下反应的化学方程式为2Mg+CO2 2MgO+C,
2MgO+C,
故答案为:2Mg+CO2 2MgO+C;
2MgO+C;
(4)若A、B属于同一主族的高硬度单质,A是C,甲是SiO2;乙是CO,B是Si,C是O2,A的同素异形体为石墨或无定形碳,与二氧化硅反应可制取粗硅,故答案为:制取粗硅.
分析:(1)根据化合反应的定义判断,图中化合反应的反应物都是单质,可为化合物的化合反应;
(2)若甲常温下呈液态,应为H2O,A常温下是固态非金属单质,应为碳,则乙是CO,B是H2,C是O2;若A常温下是气态非金属单质,应为F2,乙是HF,B是O2,C是H2;
(3)若甲常温下呈气态,A是常见的金属单质,应为Mg,甲是CO2;乙是Mg,B是C,C是O2;
(4)若A、B属于同一主族的高硬度单质,A是C,甲是SiO2;乙是CO,B是Si,C是O2.
点评:本题考查无机物的推断,题目难度中等,本题注意把握相关物质的转化关系,明确常见物质的性质为解答该题的关键.
(2)若甲常温下呈液态,应为H2O,A常温下是固态非金属单质,应为碳,则乙是CO,B是H2,C是O2;若A常温下是气态非金属单质,应为F2,乙是HF,B是O2,C是H2,乙的电子式为
 ,故答案为:CO;
,故答案为:CO; ;
;(3)若甲常温下呈气态,A是常见的金属单质,应为Mg,甲是CO2;乙是Mg,B是C,C是O2,A和甲在一定条件下反应的化学方程式为2Mg+CO2
 2MgO+C,
2MgO+C,故答案为:2Mg+CO2
 2MgO+C;
2MgO+C; (4)若A、B属于同一主族的高硬度单质,A是C,甲是SiO2;乙是CO,B是Si,C是O2,A的同素异形体为石墨或无定形碳,与二氧化硅反应可制取粗硅,故答案为:制取粗硅.
分析:(1)根据化合反应的定义判断,图中化合反应的反应物都是单质,可为化合物的化合反应;
(2)若甲常温下呈液态,应为H2O,A常温下是固态非金属单质,应为碳,则乙是CO,B是H2,C是O2;若A常温下是气态非金属单质,应为F2,乙是HF,B是O2,C是H2;
(3)若甲常温下呈气态,A是常见的金属单质,应为Mg,甲是CO2;乙是Mg,B是C,C是O2;
(4)若A、B属于同一主族的高硬度单质,A是C,甲是SiO2;乙是CO,B是Si,C是O2.
点评:本题考查无机物的推断,题目难度中等,本题注意把握相关物质的转化关系,明确常见物质的性质为解答该题的关键.

练习册系列答案
相关题目
A、B、C、D、E五种元素,A元素的周期数、主族数、原子序数相同;B的基态原子核外有3种能量不同的原子轨道,且每种轨道中的电子数相同;C元素的电离能如图所示;D元素的价电子构型为nsnnpn+2;E是第4周期的过渡金属元素,血红蛋白中的E元素与BD形成的配位键比与D2形成的配位键强.E单质与BD形成的配合物E(BD)5,常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.

(1)E(BD) 5晶体属于 (填晶体类型).
(2)A元素和B元素组成的化合物分子之间 (填“有”或“没有”)形成氢键.
(3)基态E原子的电子排布式为 .
(4)B、C、D三种元素的电负性由大到小的顺序是 (填元素符号).
(5)C2和B2A2的分子中根据电子云重叠的方式不同,都包含的共价键类型有 .
(6)已知原子数和电子数相同的微粒叫等电子体,等电子体的结构相似.根据下表数据,说明BD分子比C2分子活泼的原因 .

(1)E(BD) 5晶体属于
(2)A元素和B元素组成的化合物分子之间
(3)基态E原子的电子排布式为
(4)B、C、D三种元素的电负性由大到小的顺序是
(5)C2和B2A2的分子中根据电子云重叠的方式不同,都包含的共价键类型有
(6)已知原子数和电子数相同的微粒叫等电子体,等电子体的结构相似.根据下表数据,说明BD分子比C2分子活泼的原因
| X-Y | X=Y | X≡Y | |
| BD的键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| C2的键能(kJ?mol-1) | 154.8 | 418.4 | 941.7 |



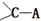 所得ABCD的结构式为
所得ABCD的结构式为