题目内容
[化学-选修物质结构和性质]
下表为部分短周期非金属元素的性质或原子结构,已知A-D的原子序数依次增大.
请结合表中信息完成下列各小题(答题时用所对应的元素符号)
A:(1)写出C原子的电子排布图
(2)A、B、C、D的第一电离能由大到小的顺序为
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和.已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发.
(4)ABC的结构式是 .向其中插入一个D原子,若形成配位键(用→表示)则ABCD的结构式为 分子中C的原子的杂化类型是 ;若无配位键则ABCD的结构式为 分子中D原子的杂化类型为 .
(5)BD2的电子式是 将D原子换成等电子的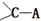 所得ABCD的结构式为 ,分子中C原子的杂化类型是 .
所得ABCD的结构式为 ,分子中C原子的杂化类型是 .
(6)在ABCD的三种可能结构中B原子的杂化类型 (填“相同”或“不相同”)
下表为部分短周期非金属元素的性质或原子结构,已知A-D的原子序数依次增大.
| 元素编号 | 元素性质或原子结构 |
| A | A原子所处的周期数、族序数、原子序数均相等 |
| B | 核外电子有6种不同运动状态 |
| C | 最简单氢化物的水溶液呈碱性 |
| D | 基态原子的S轨道电子数等于P轨道电子数 |
A:(1)写出C原子的电子排布图
(2)A、B、C、D的第一电离能由大到小的顺序为
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和.已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发.
(4)ABC的结构式是
(5)BD2的电子式是
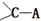 所得ABCD的结构式为
所得ABCD的结构式为(6)在ABCD的三种可能结构中B原子的杂化类型
分析:短周期非金属元素的性质或原子结构,且A-D的原子序数依次增大.A原子所处的周期数、族序数、原子序数均相等,则A为氢元素;B核外电子有6种不同运动状态,即核外电子数为6,则B为碳元素;C最简单氢化物的水溶液呈碱性,则C为氮元素;D基态原子的S轨道电子数等于P轨道电子数,则其核外电子排布式为1s22s22p4或1s22s22p63s2,为非金属性元素,则其核外电子排布式为1s22s22p4,则D为氧元素,据此解答.
解答:解:短周期非金属元素的性质或原子结构,且A-D的原子序数依次增大.A原子所处的周期数、族序数、原子序数均相等,则A为氢元素;B核外电子有6种不同运动状态,即核外电子数为6,则B为碳元素;C最简单氢化物的水溶液呈碱性,则C为氮元素;D基态原子的S轨道电子数等于P轨道电子数,则其核外电子排布式为1s22s22p4或1s22s22p63s2,为非金属性元素,则其核外电子排布式为1s22s22p4,则D为氧元素,
(1)C为氮元素,原子核外有7个电子,原子的电子排布图为 ,
,
故答案为: ;
;
(2)同周期自左而右第一电离能呈增大趋势,但N元素氧原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,非金属性越强第一电离能越大,故第一电离能N>O>C>H,
故答案为:N>O>C>H;
(3)C的最简单氢化物为NH3,其水溶液中NH3?H2O发生电离NH3?H2O?NH4++OH-,使溶液呈碱性,
故答案为:NH3?H2O?NH4++OH-;
(4)HCN分子中C原子与N原子之间形成3对共用电子对,C原子与H原子之间形成1对共用电子对,故HCN的结构式是为H-C≡N,向其中插入一个O原子,若形成配位键,N原子通过孤对电子、O原子通过空轨道形成配位键,则HCNO的结构式为H-C≡N→O,分子中N原子成1个σ键、含1对孤对电子,N原子采取sp杂化;若无配位键则HCNO中,O原子应在H-C≡N中H-C键之间插入,其结构式为H-O-C≡N,分子中O原子成2个σ键、含2对孤对电子,O原子采取sp3杂化,
故答案为:H-C≡N;H-C≡N→O;sp;H-O-C≡N;sp3;
(5)CO2的电子式是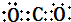 ,将D原子换成等电子的
,将D原子换成等电子的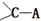 ,根据稳定结构可知,N与C之间形成2对共用电子对,故所得ABCD的结构式为 H-N=C=O,分子中N原子成2个σ键、含1对孤对电子,N原子采取sp2杂化,
,根据稳定结构可知,N与C之间形成2对共用电子对,故所得ABCD的结构式为 H-N=C=O,分子中N原子成2个σ键、含1对孤对电子,N原子采取sp2杂化,
故答案为: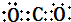 ;H-N=C=O;sp2;
;H-N=C=O;sp2;
(6)在ABCD的三种可能结构中C原子都成2个σ键、不含孤对电子,C原子均采取sp杂化,
故答案为:相同.
(1)C为氮元素,原子核外有7个电子,原子的电子排布图为
 ,
,故答案为:
 ;
;(2)同周期自左而右第一电离能呈增大趋势,但N元素氧原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,非金属性越强第一电离能越大,故第一电离能N>O>C>H,
故答案为:N>O>C>H;
(3)C的最简单氢化物为NH3,其水溶液中NH3?H2O发生电离NH3?H2O?NH4++OH-,使溶液呈碱性,
故答案为:NH3?H2O?NH4++OH-;
(4)HCN分子中C原子与N原子之间形成3对共用电子对,C原子与H原子之间形成1对共用电子对,故HCN的结构式是为H-C≡N,向其中插入一个O原子,若形成配位键,N原子通过孤对电子、O原子通过空轨道形成配位键,则HCNO的结构式为H-C≡N→O,分子中N原子成1个σ键、含1对孤对电子,N原子采取sp杂化;若无配位键则HCNO中,O原子应在H-C≡N中H-C键之间插入,其结构式为H-O-C≡N,分子中O原子成2个σ键、含2对孤对电子,O原子采取sp3杂化,
故答案为:H-C≡N;H-C≡N→O;sp;H-O-C≡N;sp3;
(5)CO2的电子式是
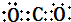 ,将D原子换成等电子的
,将D原子换成等电子的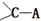 ,根据稳定结构可知,N与C之间形成2对共用电子对,故所得ABCD的结构式为 H-N=C=O,分子中N原子成2个σ键、含1对孤对电子,N原子采取sp2杂化,
,根据稳定结构可知,N与C之间形成2对共用电子对,故所得ABCD的结构式为 H-N=C=O,分子中N原子成2个σ键、含1对孤对电子,N原子采取sp2杂化,故答案为:
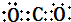 ;H-N=C=O;sp2;
;H-N=C=O;sp2;(6)在ABCD的三种可能结构中C原子都成2个σ键、不含孤对电子,C原子均采取sp杂化,
故答案为:相同.
点评:本题考查物质结构与性质,涉及核外电子排布规律、电离能、常用化学用语、杂化理论等,难度中等,注意根据σ键、孤对电子判断杂化方式(或计算价层电子对数判断杂化方式).

练习册系列答案
相关题目
 (2011?新余二模)化学--选修物质结构与性质
(2011?新余二模)化学--选修物质结构与性质
 [化学-选修物质结构与性质]
[化学-选修物质结构与性质]