题目内容
12.有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请回答问题.| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第八列 |
(2)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形;
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
 ,该同学所画的电子排布图违背了泡利原理;
,该同学所画的电子排布图违背了泡利原理;(4)D是P,E是Cl(填元素符号);
(5)G位于第Ⅷ族,G3+电子排布式为ls22s22p63s23p63d5;
(6)第二、三、四周期中与F同一族的所有元素分别与E元素形成化合物,其晶体的熔点由高到低的排列顺序为(写化学式)LiCl>NaCl>KCl,原因是LiCl、NaCl、KCl均为离子晶体,因为Li+、Na+、K+的半径依次增大,LiCl、NaCl、KCl的晶格能依次减小,故熔点依次降低.
分析 A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大,其中:
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素,A为H元素;
B元素原子的核外p电子数比s电子数少1,B有2个电子层,为1s22s22p3,故B为N元素;
由C原子的第一至第四电离能数据可知,第三电离能剧增,故C为+2,原子序数大于N元素,故C为Mg元素;
D处于第三周期,D原子核外所有p轨道全满或半满,最外层排布为3s23p3,故D为P元素;
E处于第三周期,E元素的主族序数与周期数的差为4,E处于第ⅦA族,故E为Cl元素;
F是前四周期中电负性最小的元素,F为第四周期元素,故F为K元素,G在第四周期周期表的第八列,G为Fe元素.
解答 解:A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大,其中:
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素,A为H元素;
B元素原子的核外p电子数比s电子数少1,B有2个电子层,为1s22s22p3,故B为N元素;
由C原子的第一至第四电离能数据可知,第三电离能剧增,故C为+2,原子序数大于N元素,故C为Mg元素;
D处于第三周期,D原子核外所有p轨道全满或半满,最外层排布为3s23p3,故D为P元素;
E处于第三周期,E元素的主族序数与周期数的差为4,E处于第ⅦA族,故E为Cl元素;
F是前四周期中电负性最小的元素,F为第四周期元素,故F为K元素,G在第四周期周期表的第八列,G为Fe元素.
(1)NH4Cl属于离子化合物,是由NH4+与Cl-两种粒构成,故答案为:NH4+、Cl-;
(2)B为N元素,核外电子排布式为1s22s22p3,基态原子中能量最高的电子处于2p能级,有3个电子,其电子云在空间有3个方向,原子轨道呈纺锤形,故答案为:3,纺锤;
(3)某同学根据上述信息,推断C基态原子的核外电子排布为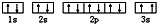 ,该同学所画的电子排布图中3s能级,2个电子自旋方向相同,违背了泡利原理,故答案为:泡利原理;
,该同学所画的电子排布图中3s能级,2个电子自旋方向相同,违背了泡利原理,故答案为:泡利原理;
(4)由上述分析可知,D为P元素、E为Cl,故答案为:P;Cl;
(5)G为Fe元素,是26号元素,位于第四周期第Ⅷ族,Fe3+电子排布式为ls22s22p63s23p63d5,故答案为:第Ⅷ;ls22s22p63s23p63d5;
(6)第二、三、四周期中与K同一族的所有元素分别与Cl元素形成化合物为:LiCl、NaCl、KCl,LiCl、NaCl、KCl均为离子晶体,因为Li+、Na+、K+的半径依次增大,LiCl、NaCl、KCl的晶格能依次减小,故熔点依次降低,故由高到低的排列顺序为:LiCl>NaCl>KCl>HCl;
故答案为:LiCl>NaCl>KCl;LiCl、NaCl、KCl均为离子晶体,因为Li+、Na+、K+的半径依次增大,LiCl、NaCl、KCl的晶格能依次减小,故熔点依次降低.
点评 本题是对物质结构的考查,涉及核外电子排布、电离能、物质晶体类型与性质等,难度中等,推断元素是解题的关键,注意基础知识的掌握.

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案①溶解②过滤③蒸发④加入适量HCl溶液⑤加入过量BaCl2溶液⑥加入过量Na2CO3溶液⑦加入过量NaOH溶液
正确的操作顺序是( )
| A. | ①⑤⑥⑦②④③ | B. | ①⑤⑦⑥②④③ | C. | ①⑦⑤⑥②④③ | D. | A或B或C |
2min后,反应达到平衡,生成C为1.6mol.则下列分析正确的是( )
| A. | 若反应开始时容器体积为2 L,则v(C)=0.4mol•L-1•min-1 | |
| B. | 若该反应在恒温恒容下进行,放出热量将增加 | |
| C. | 若2 min后,向容器中再投入等物质的量A、C,则B的转化率不变 | |
| D. | 若在恒压绝热条件下反应,平衡后n(C)<1.6mol |
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$的比值将减小(填“增大”、“减小”或“无法确定”).
(3)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)(填“>”、“<”或“=”).
(4)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液完全中和,则消耗的NaOH溶液的体积大小关系为:V(甲)<V(乙)(填“>”、“<”或“=”).
(5)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3×10-8 |
| K2 | -- | 5.6×10-11 | -- |
A.HCO${\;}_{3}^{-}$ B.CO${\;}_{3}^{2-}$ C.ClO- D.CH3COO-
写出下列反应的离子方程式:
CH3COOH+NaCO2(少量):2CH3COOH+CO32-=H2O+CO2↑+2CH3COO-;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
| A. | 向某溶液中滴加盐酸酸化的Ba(NO3)2溶液,有白色沉淀生成,则该溶液中一定含有SO42- | |
| B. | 用饱和NaHCO3溶液除去CO2气体中混有的少量SO2 | |
| C. | 将产生的气体依次通过足量的溴水和澄清石灰水,检验浓H2SO4与木炭反应生成的气体产物 | |
| D. | 实验室制取氢气,为了加快反应速率,可向稀硫酸中滴加少量Cu(NO3)2 |
| A. | 元素周期表中有8个主族 | |
| B. | ⅠA族中的元素都是金属元素 | |
| C. | 第三周期有8种元素 | |
| D. | 短周期元素是指第一、二周期含有的全部元素 |
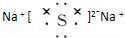 .
.