题目内容
2.关于元素周期表的说正确的是( )| A. | 元素周期表中有8个主族 | |
| B. | ⅠA族中的元素都是金属元素 | |
| C. | 第三周期有8种元素 | |
| D. | 短周期元素是指第一、二周期含有的全部元素 |
分析 A.元素周期表中有7个主族;
B.ⅠA族包括H元素;
C.第三周期的元素原子序数从11~18;
D.短周期元素为前三周期元素.
解答 解:A.元素周期表中有7个主族、7个副族、1个零族和1个Ⅷ族,故A正确;
B.ⅠA族包括H元素,为非金属元素,故B错误;
C.第三周期的元素原子序数从11~18,分别为Na、Mg、Al、Si、P、S、Cl、Ar等元素,共8种,故C正确;
D.短周期元素为前三周期元素,故D错误.
故选C.
点评 本题考查元素周期表与结构,为高频考点,侧重双基的考查,难度不大,学习中对元素周期表要熟悉.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
12.有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请回答问题.
(1)已知BA4E为离子化合物,是由NH4+、Cl-两种微粒构成的(填化学符号);
(2)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形;
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,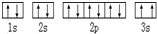 ,该同学所画的电子排布图违背了泡利原理;
,该同学所画的电子排布图违背了泡利原理;
(4)D是P,E是Cl(填元素符号);
(5)G位于第Ⅷ族,G3+电子排布式为ls22s22p63s23p63d5;
(6)第二、三、四周期中与F同一族的所有元素分别与E元素形成化合物,其晶体的熔点由高到低的排列顺序为(写化学式)LiCl>NaCl>KCl,原因是LiCl、NaCl、KCl均为离子晶体,因为Li+、Na+、K+的半径依次增大,LiCl、NaCl、KCl的晶格能依次减小,故熔点依次降低.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第八列 |
(2)B基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形;
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
 ,该同学所画的电子排布图违背了泡利原理;
,该同学所画的电子排布图违背了泡利原理;(4)D是P,E是Cl(填元素符号);
(5)G位于第Ⅷ族,G3+电子排布式为ls22s22p63s23p63d5;
(6)第二、三、四周期中与F同一族的所有元素分别与E元素形成化合物,其晶体的熔点由高到低的排列顺序为(写化学式)LiCl>NaCl>KCl,原因是LiCl、NaCl、KCl均为离子晶体,因为Li+、Na+、K+的半径依次增大,LiCl、NaCl、KCl的晶格能依次减小,故熔点依次降低.
13.下列化学用语的使用正确的是( )
| A. | 氟离子的结构示意图: | B. | 甲烷的比例模型: | ||
| C. | NaCl的电子式: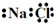 | D. | 乙炔的结构简式:CHCH |
10.下列元素中属于第三周期且原子半径最大的是( )
| A. | F | B. | N | C. | Na | D. | Al |
17.下列反应中属于吸热反应的是( )
| A. | 生石灰和水的反应 | |
| B. | 铁丝在纯氧中点燃 | |
| C. | 锌与盐酸反应 | |
| D. | 氢氧化钡晶体与氯化铵晶体混合搅拌 |
7.在2L密闭容器中,发生反应2A+B=2C+D,若最初A、B都是8mol,在前10s 内A 的平均速率为0.24mol/(L?s),则10s时B的物质的量是( )
| A. | 2.4mol | B. | 3.2mol | C. | 4.8mol | D. | 5.6mol |
14.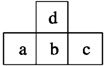 如图为周期表中短周期的一部分.已知a原子的最外层上的电子数目是次外层电子数目的一半,下列说法中不正确的是( )
如图为周期表中短周期的一部分.已知a原子的最外层上的电子数目是次外层电子数目的一半,下列说法中不正确的是( )
 如图为周期表中短周期的一部分.已知a原子的最外层上的电子数目是次外层电子数目的一半,下列说法中不正确的是( )
如图为周期表中短周期的一部分.已知a原子的最外层上的电子数目是次外层电子数目的一半,下列说法中不正确的是( )| A. | 元素b的最高价氧化物的水化物的酸性比c的弱 | |
| B. | 元素d的原子半径比a的小 | |
| C. | 元素a单质在空气中燃烧会导致“温室效应” | |
| D. | 元素a的单质是一种良好的半导体材料 |
11.苯不能发生的化学反应类型是( )
| A. | 取代反应 | B. | 酯化反应 | C. | 加成反应 | D. | 氧化反应 |
12.下列过程属于物理变化的是( )
| A. | 海水淡化 | B. | 石油裂化 | C. | 煤的干馏 | D. | 煤的气化 |