题目内容
17.可逆反应mA(s)+nB(g)?cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(p)的关系如下图所示(T2>T1),下列叙述错误的是( )
| A. | 达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动 | |
| B. | 达到平衡后,若使温度升高,化学平衡向逆反应方向移动 | |
| C. | 化学方程式中n<c+f | |
| D. | 达到平衡后,若使用催化剂,C的体积分数不变 |
分析 T2达到平衡时间短,温度较高,而C%含量低,则正反应方向放热,P2达到平衡时间短,压强较大,而C%含量低,则m+n<e+f,催化剂不影响平衡移动,据此判断.
解答 解:A、A是固体,加A的量,不影响平衡移动,故A错误;
B、T2达到平衡时间短,温度较高,而C%含量低,正反应方向放热,升温平衡逆向移动,故B正确;
C、P2达到平衡时间短,压强较大,而C%含量低,则n<e+f,故C正确;
D、若使用催化剂,平衡不移动,C的体积分数不变,故D正确;
故选A.
点评 本题考查化学平衡图象、影响平衡的因素、影响因素等,难度不大,注意掌握平衡移动原理,根据图象判断温度和压强对平衡移动的影响.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
7.${\;}_{6}^{13}$C-NMR(核磁共振)可用于含碳化合物的结构分析.下列有关${\;}_{6}^{13}$C的说法正确的是( )
| A. | ${\;}_{6}^{13}$C的质量数是13,原子序数是6,核内有6个中子 | |
| B. | ${\;}_{6}^{13}$C与金刚石、石墨、C60等互为同素异形体 | |
| C. | ${\;}_{6}^{13}$C与${\;}_{6}^{12}$C是两种不同的碳元素 | |
| D. | ${\;}_{6}^{13}$C是碳的一种核素,与${\;}_{6}^{12}$C互为同位素 |
8.如图为元素周期表的一部分,下列有关B、W、X、Y、Z五种元素的叙述中正确的是( )
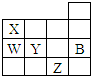

| A. | 常压下,五种元素的单质中,Z单质的沸点最高 | |
| B. | X的氢化物沸点比W的氢化物沸点高 | |
| C. | Y元素氧化物的水化物酸性比W的强 | |
| D. | Y、Z的简单阴离子的电子层结构都与B原子的相同 |
5.下列反应对应的离子方程式中正确的是( )
| A. | FeCl3溶液中加入铁粉:Fe+Fe3+═2Fe2+ | |
| B. | NH4HSO4溶液中加入少量NaOH:NH4++OH-═NH3•H2O | |
| C. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 氯气通入Na2SO3溶液中:Cl2+SO32-+H2O═SO42-+2H++2Cl- |
12.下列关于反应2Na2O2+2H2O═4NaOH+O2↑的说法正确的是( )
| A. | 过氧化钠是氧化剂,水是还原剂 | B. | Na2O2是还原剂,水是氧化剂 | ||
| C. | 过氧化钠既是氧化剂又是还原剂 | D. | 水既是氧化剂又是还原剂 |
2.下列化学用语正确的是( )
| A. | 氯原子的结构示意图: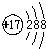 | |
| B. | 硫酸的电离方程式:H2SO4═H2++SO42- | |
| C. | 苏打粉的化学式:NaHCO3 | |
| D. | 明矾的化学式:KAl(SO4)2•12H2O |
9.下列实验或操作合理的是( )
| A. | 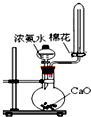 制氨气 | B. | 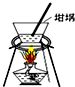 蒸发、浓缩、结晶 | ||
| C. | 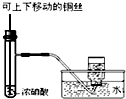 制备并收集少了二氧化氮 | D. | 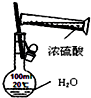 浓硫酸稀释 |
6.下列离子检验的操作或说法正确的是( )
| A. | 某溶液加入几滴KSCN溶液后不变色再滴加几滴氯水后,溶液变红,说明该溶液一定有Fe2+ | |
| B. | 某溶液滴加AgNO3溶液产生白色沉淀,说明该溶液一定含Cl- | |
| C. | 某溶液加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,说明该溶液一定有CO32- | |
| D. | 某溶液滴加盐酸酸化的BaCl2溶液后,有白色沉淀产生,说明该溶液一定含SO42- |
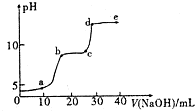 某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.
某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.