题目内容
5.下列反应对应的离子方程式中正确的是( )| A. | FeCl3溶液中加入铁粉:Fe+Fe3+═2Fe2+ | |
| B. | NH4HSO4溶液中加入少量NaOH:NH4++OH-═NH3•H2O | |
| C. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 氯气通入Na2SO3溶液中:Cl2+SO32-+H2O═SO42-+2H++2Cl- |
分析 A.离子方程式两边正电荷不相等;
B.氢离子优先结合氢氧根离子,氢氧化钠少量,铵根离子不参与反应;
C.2mol钠完全反应生成1mol氢气,该反应不满足电子守恒;
D.氯气具有强氧化性,能够与亚硫酸钠发生氧化还原反应生成硫酸钠和HCl.
解答 解:A.FeCl3溶液中加入铁粉,反应生成氯化亚铁,正确的离子方程式为:Fe+2Fe3+═3Fe2+,故A错误;
B.NH4HSO4溶液中加入少量NaOH,氢离子优先结合氢氧根离子,反应生成硫酸铵和硫酸钠,正确的离子方程式为:H++OH-═H2O,故B错误;
C.钠与水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故C错误;
D.氯气通入Na2SO3溶液中,二者发生氧化还原反应,反应的离子方程式为:Cl2+SO32-+H2O═SO42-+2H++2Cl-,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
15.取100mL 0.3mol/L的硫酸注入500mL容量瓶中,加水稀释至刻度线,该溶液中H+的物质的量浓度是( )
| A. | 0.06mol/L | B. | 0.12mol/L | C. | 0.03mol/L | D. | 0.24mol/L |
16.铜的冶炼大致可分为:
(1)富集,将硫化物矿进行浮选;
(2)焙烧,主要反应为2Cu+FeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
(3)制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2;
(4)电解精炼.
下列说法正确的是( )
(1)富集,将硫化物矿进行浮选;
(2)焙烧,主要反应为2Cu+FeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
(3)制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2;
(4)电解精炼.
下列说法正确的是( )
| A. | 上述灼烧过程的尾气均可直接排到空气中 | |
| B. | 由6 mol CuFeS2生成6 mol Cu,上述共消耗15 mol O2 | |
| C. | 在反应2Cu2O+Cu2S═6Cu+SO2中,作氧化剂的只有Cu2O | |
| D. | 电解精炼时,粗铜应与外电源正极相连 |
13.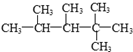 是由一种单烯烃加氢而成的,那么原烯烃的可能结构有( )
是由一种单烯烃加氢而成的,那么原烯烃的可能结构有( )
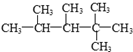 是由一种单烯烃加氢而成的,那么原烯烃的可能结构有( )
是由一种单烯烃加氢而成的,那么原烯烃的可能结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
10.图表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素.下列说法正确的是( )
| X | ||
| Y | z | R |
| W |
| A. | 五种元素的原子最外层电子数一定都大于2 | |
| B. | Z的氧化物与X单质不可能发生置换反应 | |
| C. | X、Z原子序数可能相差18 | |
| D. | Z可能是氯元素 |
17.可逆反应mA(s)+nB(g)?cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(p)的关系如下图所示(T2>T1),下列叙述错误的是( )


| A. | 达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动 | |
| B. | 达到平衡后,若使温度升高,化学平衡向逆反应方向移动 | |
| C. | 化学方程式中n<c+f | |
| D. | 达到平衡后,若使用催化剂,C的体积分数不变 |
14.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 1 mol乙炔分子所含的共用电子对总数为5NA | |
| B. | 1 mol甲基(-CH3 )所含的电子总数为9NA | |
| C. | 0.5 mol 1,3-丁二烯分子中含有碳碳双键总数为NA | |
| D. | 标准状况下,22.4L己烷完全燃烧所生成的气态产物的分子数为7NA |
15.下列解释事实的化学方程式或离子方程式中错误的是( )
| A. | 在复盐NH4Fe(SO4)2溶液中加入过量的Ba(OH)2溶液:NH4++Fe3++2SO42-+2Ba2++4OH-═2BaSO4↓+Fe(OH)3↓+NH3•H2O | |
| B. | 在盐碱地(含较多NaCl、Na2CO3)上通过施加适量CaSO4可降低土壤的碱性:CaSO4+Na2CO3═CaCO3+Na2SO4 | |
| C. | 在燃煤时加入适量石灰石粉末,可减少SO2的排放:CaCO3+SO2═CaSO3+CO2 | |
| D. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2H++2I-+H2O2═I2+2H2O |

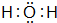 D 的原子结构示意图
D 的原子结构示意图 .
.