题目内容
可用呋喃为主要原料合成聚酰胺纤维(尼龙-66,含有-CO-NH-结构),合成路线如下:
已知:RCl
RCN;CH3CONH2名称是乙酰胺.回答下列问题:
(1)写出反应类型:反应③ ;反应⑥ .
(2)写出A、B的结构筒式:
A ;B .
(3)写出有关的化学方程式:反应② ;反应⑥ .
(4)呋喃与苯相似,也具有芳香性,则可推知呋喃能发生的化学反应是 (选填编号).
a.使溴水褪色 b.使酸性高锰酸钾溶液褪色 c.与溴发生取代反应 d.发生l,4加成反应
(5)写出乙酰胺制取乙腈(CH3C≡N)的化学方程式: .
(6)H是A的同分异构体,被酸性高锰酸钾溶液氧化生成丙二酸和CO2,则H的结构简式为 .

已知:RCl
| NaCN |
(1)写出反应类型:反应③
(2)写出A、B的结构筒式:
A
(3)写出有关的化学方程式:反应②
(4)呋喃与苯相似,也具有芳香性,则可推知呋喃能发生的化学反应是
a.使溴水褪色 b.使酸性高锰酸钾溶液褪色 c.与溴发生取代反应 d.发生l,4加成反应
(5)写出乙酰胺制取乙腈(CH3C≡N)的化学方程式:
(6)H是A的同分异构体,被酸性高锰酸钾溶液氧化生成丙二酸和CO2,则H的结构简式为
考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)(2)(3)反应①为加成反应,可知A为 ,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为
,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为 ,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙
,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙 ;
;
(4)呋喃与苯相似,也具有芳香性,不存在典型的碳碳双键,结合苯的性质进行判断;
(5)根据己二酰胺脱水得到 ,可知乙酰胺脱水得到乙腈(CH3C≡N);
,可知乙酰胺脱水得到乙腈(CH3C≡N);
(6)H是A的同分异构体,二者分子式相同,被酸性高锰酸钾溶液氧化生成丙二酸和CO2,H存在-CH2OH,还含有碳碳双键.
 ,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为
,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为 ,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙
,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙 ;
;(4)呋喃与苯相似,也具有芳香性,不存在典型的碳碳双键,结合苯的性质进行判断;
(5)根据己二酰胺脱水得到
 ,可知乙酰胺脱水得到乙腈(CH3C≡N);
,可知乙酰胺脱水得到乙腈(CH3C≡N);(6)H是A的同分异构体,二者分子式相同,被酸性高锰酸钾溶液氧化生成丙二酸和CO2,H存在-CH2OH,还含有碳碳双键.
解答:
解:反应①为加成反应,可知A为 ,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为
,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为 ,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙
,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙 ,
,
(1)由上述分析可知,反应③属于取代反应,反应⑥属于缩聚反应,故答案为:取代反应;缩聚反应;
(2)由上述分析可知,A的结构简式为 ,B的结构简式为
,B的结构简式为 ,故答案为:
,故答案为: ;
; ;
;
(3)反应②的方程式为: ,
,
反应⑥的化学方程式为: ,
,
故答案为: ;
; ;
;
(4)呋喃与苯相似,也具有芳香性,不存在典型的碳碳双键,结合苯的性质可知:
a.不能使溴水褪色,故a错误;
b.不能使酸性高锰酸钾溶液褪色,故b错误;
c.与溴在催化剂的条件下,可以发生取代反应,故c正确;
d.不存在典型的碳碳双键,不能发生l,4加成反应,故d错误,
故答案为:c;
(5)根据己二酰胺脱水得到 ,可知乙酰胺制备乙腈(CH3C≡N)的化学方程式为:CH3CONH2
,可知乙酰胺制备乙腈(CH3C≡N)的化学方程式为:CH3CONH2
CH3CN+H2O,故答案为:CH3CONH2
CH3CN+H2O;
(6)H是A的同分异构体,二者分子式相同,被酸性高锰酸钾溶液氧化生成丙二酸和CO2,H存在-CH2OH,还含有碳碳双键,符合条件的H的结构简式为:CH2=CHCH2CH2OH,故答案为:CH2=CHCH2CH2OH.
 ,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为
,反应②先发生开环加成反应,然后再被氯原子取代羟基得到1,4-二氯丁烷,反应③发生信息中反应,-Cl原子被-CN取代得到B为 ,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙
,反应④为B与氢气发生加成反应得到己二胺,反应⑤为水解反应,己二胺与己二酸发生缩聚反应得到尼龙 ,
,(1)由上述分析可知,反应③属于取代反应,反应⑥属于缩聚反应,故答案为:取代反应;缩聚反应;
(2)由上述分析可知,A的结构简式为
 ,B的结构简式为
,B的结构简式为 ,故答案为:
,故答案为: ;
; ;
;(3)反应②的方程式为:
 ,
,反应⑥的化学方程式为:
 ,
,故答案为:
 ;
; ;
;(4)呋喃与苯相似,也具有芳香性,不存在典型的碳碳双键,结合苯的性质可知:
a.不能使溴水褪色,故a错误;
b.不能使酸性高锰酸钾溶液褪色,故b错误;
c.与溴在催化剂的条件下,可以发生取代反应,故c正确;
d.不存在典型的碳碳双键,不能发生l,4加成反应,故d错误,
故答案为:c;
(5)根据己二酰胺脱水得到
 ,可知乙酰胺制备乙腈(CH3C≡N)的化学方程式为:CH3CONH2
,可知乙酰胺制备乙腈(CH3C≡N)的化学方程式为:CH3CONH2 | 一定条件 |
| 一定条件 |
(6)H是A的同分异构体,二者分子式相同,被酸性高锰酸钾溶液氧化生成丙二酸和CO2,H存在-CH2OH,还含有碳碳双键,符合条件的H的结构简式为:CH2=CHCH2CH2OH,故答案为:CH2=CHCH2CH2OH.
点评:本题考查有机物推断、有机反应类型、同分异构体、有机反应方程式书写等,是对有机化学的综合考查,(4)中注意根据苯的性质进行迁移解答,难度中等.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
下列物质属于含有共价键的离子化合物的是( )
| A、MgCl2 |
| B、Br2 |
| C、KOH |
| D、H2S |
下列离子方程式书写正确的是( )
| A、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
| C、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| D、NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
下列说法中正确的是( )
| A、加热胆矾失去结晶水,得到白色的无水硫酸铜,这一过程叫风化 |
| B、家用石碱(Na2CO3?10H2O)久置后,有块状变成粉末状,这一变化是风化的结果 |
| C、白色的无水硫酸铜粉末遇水形成蓝色的硫酸铜那个晶体,这一过程叫潮解 |
| D、从冰箱中取出物品,表面很快出现水珠,这种现象叫潮解 |
用可再生的物质制备乙酸乙酯的绿色合成路线之一如图所示:
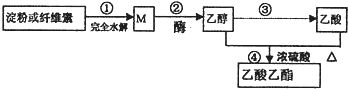
下列说法正确的是( )

下列说法正确的是( )
| A、常温下,M能与银氨溶液发生反应 |
| B、④的反应类型属于酯化反应,不属于取代反应 |
| C、用饱和碳酸钾溶液能鉴别乙醇、乙酸和乙酸乙酯 |
| D、淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体 |
已知,mg Al在足量氯气中燃烧,生成固体的质量为(m+21.3)g,若将mgAl投入总质量为95.2g的NaOH水溶液中恰好完全反应,则所得溶液中溶质的质量分数为( )
| A、5.4% | B、8.0% |
| C、16.3% | D、16.4% |