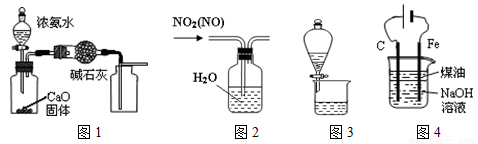
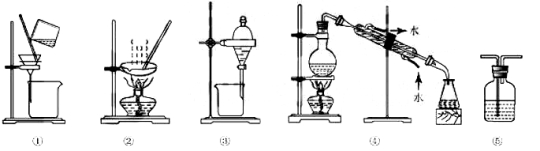
题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.0.1mol·L-1的Na2CO3溶液中,阴离子的总数目大于0.1NA
B.常温下,46 g NO2和N2O4混合气体中含有的分子总数为2NA
C.标准状况下,22.4L的HF含有NA个分子
D.标准状况下,10g的庚烷分子中含有2.2NA个共价键
D
【解析】
试题分析:A.只有浓度缺少体积,无法计算微粒的物质的量,错误;B.常温下,46 g NO2的分子数是NA个,46 g N2O4气体中含有的分子总数为0.5NA,所以混合气体的分子数小于NA个,错误;C.标准状况下,HF分子之间存在氢键,一聚合分子形式存在,因此22.4L的HF含有分子多于NA个,错误;D.标准状况下,10g的庚烷C7H16分子中含有的共价键数是(10g ÷100g/mol)×22NA=2.2NA个共价键,正确。
考点:考查阿伏加德罗常数的计算的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 g
g  %,则x=2b
%,则x=2b %
%