题目内容
下列实验中,所选装置或实验设计合理的是
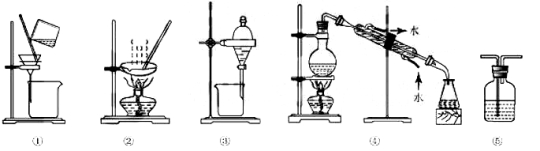
A.图⑤ 所示装置中盛有饱和Na2SO3溶液除去SO2中含有的少量HCl
B.用乙醇提取溴水中的溴选择图③所示装置
C.用图①和② 所示装置进行粗盐提纯
D.用图④所示装置进行石油分馏实验制取丁烯
C
【解析】
试题分析:A、二氧化硫与Na2SO3溶液反应,则应用图⑤所示装置中盛有饱和NaHSO3溶液除去SO2中含有的少量HCl,故A错误;B、乙醇与水混溶,不能作萃取剂,应选择苯或四氯化碳,故B错误;C、粗盐提纯需要进行溶解、过滤、蒸发操作,①为过滤装置,②为蒸发装置,故C正确;D、进行石油分馏实验,需要温度计测定馏分的温度,则不能完成实验,故D错误。
考点:本题考查化学实验方案的评价。

练习册系列答案
相关题目

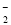 +2H2O
+2H2O 