题目内容
往明矾溶液中加入氢氧化钡溶液,下列离子方程式可能正确的是( )
| A、2A13++3SO42-+3Ba2++6OH-→2A1(OH)3↓+3BaSO4↓ |
| B、A13++2SO42-+2Ba2++3OH-→A1(OH)3↓+2BaSO4↓ |
| C、A13++SO42-+Ba2++4OH-→A1O2-+BaSO4↓+2H2O |
| D、A13++2SO42-+2Ba2++4OH-→A1O2-+2BaSO4↓+2H2O |
考点:离子方程式的书写
专题:
分析:向明矾溶液中加入过量的氢氧化钡溶液能将铝离子和硫酸根离子全部沉淀,并且生成的氢氧化铝溶于强碱中,实质是Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,
氢氧化钡恰好使铝离子沉淀,按照反应定量关系得到反应的离子方程式:2A13++3SO42-+3Ba2++6OH-=2A1(OH)3↓+3BaSO4↓,结合反应定量关系和化学式定量比分析选项判断;
氢氧化钡恰好使铝离子沉淀,按照反应定量关系得到反应的离子方程式:2A13++3SO42-+3Ba2++6OH-=2A1(OH)3↓+3BaSO4↓,结合反应定量关系和化学式定量比分析选项判断;
解答:
解:A、氢氧化钡恰好使铝离子沉淀的化学方程式为:2KAl(SO4)2+3Ba(OH)2=Al(OH)3↓+3BaSO4↓+K2SO4+3H2O,反应的离子方程式为:2A13++3SO42-+3Ba2++6OH-=2A1(OH)3↓+3BaSO4↓,故A正确;
B、不符合反应定量关系中的化学式组成比,故B错误;
C、硫酸铝钾中1mol铝离子结合2mol硫酸根离子,氢氧化钡组成比不符合,故C错误;
D、氢氧化钡溶液过量,反应化学方程式 2KAl(SO4)2+4Ba(OH)2=2KAlO2+4BaSO4↓+4H2O,反应的离子方程式为:A13++2SO42-+2Ba2++4OH-=A1O2-+2BaSO4↓+2H2O,故D正确;
故选AD.
B、不符合反应定量关系中的化学式组成比,故B错误;
C、硫酸铝钾中1mol铝离子结合2mol硫酸根离子,氢氧化钡组成比不符合,故C错误;
D、氢氧化钡溶液过量,反应化学方程式 2KAl(SO4)2+4Ba(OH)2=2KAlO2+4BaSO4↓+4H2O,反应的离子方程式为:A13++2SO42-+2Ba2++4OH-=A1O2-+2BaSO4↓+2H2O,故D正确;
故选AD.
点评:本题考查了离子方程式中定量关系的分析判断和两种方式书写方法,掌握书写方法和定量关系分析是解题关键,题目难度中等.

练习册系列答案
相关题目
Na与硫酸铜溶液反应的实验现象是( )
| A、置换出金属铜 |
| B、产生气体、生成蓝色沉淀 |
| C、生成蓝色沉淀 |
| D、产生气体、置换出金属铜 |
在同温同压下,下列各组化学反应的反应热△H,前者大于后者的是( )
| A、2H2(g)+O2(g)=2H2O(l) 2H2(g)+O2(g)=2H2O(g) | ||||
B、H2(g)+Cl2(g)=2HCl(g)
| ||||
C、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) NaOH(aq)+
| ||||
D、C(s)+
|
下列说法正确的是( )
| A、13C和14C属于同一种元素,它们互为同位素 |
| B、1H和2H是不同的粒子,但它们的质子数相等 |
| C、14C 和14N的质量数相等,它们互为同位素 |
| D、6Li和7Li的电子数相等,但中子数不相等 |
当光束通过下列分散系时,可能产生丁达尔效应的是( )
| A、NaHCO3溶液 |
| B、蔗糖溶液 |
| C、CuSO4溶液 |
| D、Fe(OH)3胶体 |
 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示. 
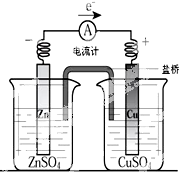 用铜片、锌片、CuSO4溶液、ZnSO4溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池.以下有关该原电池的叙述正确的是( )
用铜片、锌片、CuSO4溶液、ZnSO4溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池.以下有关该原电池的叙述正确的是( )