题目内容
在同温同压下,下列各组化学反应的反应热△H,前者大于后者的是( )
| A、2H2(g)+O2(g)=2H2O(l) 2H2(g)+O2(g)=2H2O(g) | ||||
B、H2(g)+Cl2(g)=2HCl(g)
| ||||
C、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) NaOH(aq)+
| ||||
D、C(s)+
|
考点:反应热的大小比较
专题:化学反应中的能量变化
分析:化学反应热的大小比较考虑:
正负号:放热反应△H<0,吸热反应△H>0,放出的热量越多△H越小.
反应热的大小与反应物的状态及反应物的量有关.
正负号:放热反应△H<0,吸热反应△H>0,放出的热量越多△H越小.
反应热的大小与反应物的状态及反应物的量有关.
解答:
解:A.相同量的氧气和氢气生成液态水放热更多,所以前者放出热量多,则△H小,故A错误;
B.H2(g)+Cl2(g)═2HCl(g);
H2(g)+
Cl2(g)═HCl(g),第一个反应消耗的氢气比第二个反应多,放出的热量多,所以其△H小,故B错误;
C.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);NaOH(aq)+
H2SO4(aq)═
Na2SO4(aq)+H2O(l)都表示1mol氢离子和1mol氢氧根离子生成1mol水放出的热量即中和热,所以二者△H相同,故C错误;
D.相同物质的量的C,生成CO比生成CO2放出的热量少,则△H大,故D正确;
故选D.
B.H2(g)+Cl2(g)═2HCl(g);
| 1 |
| 2 |
| 1 |
| 2 |
C.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);NaOH(aq)+
| 1 |
| 2 |
| 1 |
| 2 |
D.相同物质的量的C,生成CO比生成CO2放出的热量少,则△H大,故D正确;
故选D.
点评:本题考查反应热的大小比较,题目难度较小,注意反应热有正负号,放热反应焓变值小于0,吸热反应焓变值大于0.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、绿色食品是不含任何化学物质的食品 |
| B、Na2O2与CO2反应,Na2O2是氧化剂、CO2是还原剂 |
| C、与同浓度的硫酸反应时,NaHCO3比Na2CO3剧烈 |
| D、称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液,则放出氢气的体积(同温同压下)不相等 |
等浓度的下列溶液中,NH4+浓度最大的是( )
| A、(NH4)2SO4 |
| B、NH4Cl |
| C、(NH4)2CO3 |
| D、NH4HCO3 |
可逆反应2NO2?2NO+O2在恒容密闭容器中反应,能说明反应已达到平衡状态的是( )
①单位时间内生成n mo1O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n molNO
③混合气体的颜色不再改变
④c(NO2):c(NO):c(O2)=2:2:1
⑤混合气体的压强保持不变
⑥各物质的浓度相等.
①单位时间内生成n mo1O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n molNO
③混合气体的颜色不再改变
④c(NO2):c(NO):c(O2)=2:2:1
⑤混合气体的压强保持不变
⑥各物质的浓度相等.
| A、①③⑤ | B、②④⑤⑥ |
| C、①③④⑤⑥ | D、①②③④⑤⑥ |
往明矾溶液中加入氢氧化钡溶液,下列离子方程式可能正确的是( )
| A、2A13++3SO42-+3Ba2++6OH-→2A1(OH)3↓+3BaSO4↓ |
| B、A13++2SO42-+2Ba2++3OH-→A1(OH)3↓+2BaSO4↓ |
| C、A13++SO42-+Ba2++4OH-→A1O2-+BaSO4↓+2H2O |
| D、A13++2SO42-+2Ba2++4OH-→A1O2-+2BaSO4↓+2H2O |
科学家不久前制得一种新型分子O4.2mol O4和4mol O2含有的( )
| A、电子数相同,分子数不同 |
| B、质量相同,电子数不同 |
| C、原子数相同,质子数不同 |
| D、分子数相同,质量不同 |
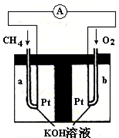 燃料电池(Fuel Cell)是一种将存在于燃料与氧化剂中的化学能直接转化为电能的发电装置.燃料和空气分别送进燃料电池,电就被奇妙地生产出来.它从外表上看有正负极和电解质等,像一个蓄电池,但实质上它不能“储电”而是一个“发电厂”.
燃料电池(Fuel Cell)是一种将存在于燃料与氧化剂中的化学能直接转化为电能的发电装置.燃料和空气分别送进燃料电池,电就被奇妙地生产出来.它从外表上看有正负极和电解质等,像一个蓄电池,但实质上它不能“储电”而是一个“发电厂”.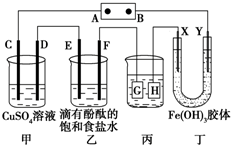 如图所示装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中的溶液都是1mol?L-1 500mL(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答:
如图所示装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中的溶液都是1mol?L-1 500mL(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答: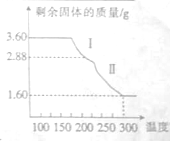 铁及铁的化合物用途非常广泛.
铁及铁的化合物用途非常广泛.