题目内容
(一)恒温恒容下,将2mol A气体和2mol B气体通入体积为2L的密闭容器中发生如下反应:2A(g)+B(g)?x C(g)+2D(s),2min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mo1?L-1.
(1)从开始反应至达到平衡状态,生成C的平均反应速率为 .
(2)x= .
(3)下列各项可作为该反应达到平衡状态的标志的是 .
A.压强不再变化 B.气体密度不再变化 C.A的消耗速率与B的消耗速率之比为2:1
(二)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g),△H
下表所列数据是该反应在不同温度下的化学平衡常数(K).
①根据表中数据可判断△H 0(填“>”、“=”或“<”).
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将 .
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
(2)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4KOH═2K2CO3+6H2O,则正极的电极反应式为 ,随着反应的不断进行溶液的pH (填“增大”“减小”或“不变”).
(3)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为 .
(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)x=
(3)下列各项可作为该反应达到平衡状态的标志的是
A.压强不再变化 B.气体密度不再变化 C.A的消耗速率与B的消耗速率之比为2:1
(二)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g),△H
下表所列数据是该反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
(2)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4KOH═2K2CO3+6H2O,则正极的电极反应式为
(3)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为
考点:化学平衡的影响因素,反应热和焓变,化学电源新型电池,反应速率的定量表示方法,化学平衡状态的判断
专题:基本概念与基本理论
分析:(一)(1)2min达到平衡,C的浓度为1.2mol/L,结合v=
计算;
(2)2min时反应达到平衡状态,此时剩余1.2mol B,计算B的反应速率,反应速率之比等于化学计量数之比;
(3)利用平衡的特征“等、定”及由此衍生的物理量来判断平衡;
(二)(1)①依据表中数据分析,随温度升高,平衡常数减小,说明平衡逆向进行;
②计算浓度商和平衡常数比较分析判断反应进行方向;
(2)原电池中负极上燃料失电子,碱性条件下,CH3OH反应生成碳酸根离子;根据电极反应判断氢氧根离子浓度的变化;
(3)根据电解池的工作原理,分析两个电极上放电的离子,并确定生成的物质.
| △c |
| △t |
(2)2min时反应达到平衡状态,此时剩余1.2mol B,计算B的反应速率,反应速率之比等于化学计量数之比;
(3)利用平衡的特征“等、定”及由此衍生的物理量来判断平衡;
(二)(1)①依据表中数据分析,随温度升高,平衡常数减小,说明平衡逆向进行;
②计算浓度商和平衡常数比较分析判断反应进行方向;
(2)原电池中负极上燃料失电子,碱性条件下,CH3OH反应生成碳酸根离子;根据电极反应判断氢氧根离子浓度的变化;
(3)根据电解池的工作原理,分析两个电极上放电的离子,并确定生成的物质.
解答:
解:(一)(1)2min达到平衡,C的浓度为1.2mol/L,由v=
=
=0.6mol/(L.min),故答案为:0.6mol/(L.min);
(2)2min时反应达到平衡状态,此时剩余1.2mol B,则B的反应速率为
=0.2mol/(L.min),由反应速率之比等于化学计量数之比可知,x=3,故答案为:3;
(3)2A(g)+B(g)
3C(g)+2D(s),
A.该反应中压强始终不变,不能判断平衡,故A错误;
B.因气体的质量在变化,则气体密度不再变化,达到平衡,故B正确;
C.A的消耗速率与B的消耗速率之比为2:1,关系始终存在,不能判断平衡,故C错误;
故答案为:B;
(二)(1)①依据表中数据分析,随温度升高,平衡常数减小,说明平衡逆向进行正反应为放热反应,△H<0;
故答案为:<;
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,CO(g)+2H2(g)?CH3OH(g),浓度商Q=
=
<K=0.270,反应正向进行;
故答案为:A;
(2)原电池放电时,甲醇失电子被氧化,应为电池负极反应,其电极反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,正极电极反应为:O2+2H2O+4e-=4OH-;已知电池总反应为:2CH3OH+3O2+4KOH=2K2CO3+6H2O,电池在放电过程中消耗氢氧根离子,所以溶液的pH减小;
故答案为:O2+2H2O+4e-=4OH-;减小;
(3)电解饱和食盐水时,阳极是氯离子失电子生成氯气的过程,电极反应式为2Cl--2e-=Cl2↑,
故答案为:2Cl--2e-=Cl2↑.
| △c |
| △t |
| 1.2mol/L |
| 2min |
(2)2min时反应达到平衡状态,此时剩余1.2mol B,则B的反应速率为
| ||
| 2min |
(3)2A(g)+B(g)
| ||
A.该反应中压强始终不变,不能判断平衡,故A错误;
B.因气体的质量在变化,则气体密度不再变化,达到平衡,故B正确;
C.A的消耗速率与B的消耗速率之比为2:1,关系始终存在,不能判断平衡,故C错误;
故答案为:B;
(二)(1)①依据表中数据分析,随温度升高,平衡常数减小,说明平衡逆向进行正反应为放热反应,△H<0;
故答案为:<;
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,CO(g)+2H2(g)?CH3OH(g),浓度商Q=
| 2 |
| 2×32 |
| 1 |
| 9 |
故答案为:A;
(2)原电池放电时,甲醇失电子被氧化,应为电池负极反应,其电极反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,正极电极反应为:O2+2H2O+4e-=4OH-;已知电池总反应为:2CH3OH+3O2+4KOH=2K2CO3+6H2O,电池在放电过程中消耗氢氧根离子,所以溶液的pH减小;
故答案为:O2+2H2O+4e-=4OH-;减小;
(3)电解饱和食盐水时,阳极是氯离子失电子生成氯气的过程,电极反应式为2Cl--2e-=Cl2↑,
故答案为:2Cl--2e-=Cl2↑.
点评:本题考查了化学反应速率,平衡常数影响因素分析判断,原电池、电解池原理的分析应用,掌握基础是关键,题目难度中等.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
可用于鉴别以下三种化合物的一组试剂是( )

①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液.

①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液.
| A、①与② | B、③与④ |
| C、①与④ | D、②与③ |
下列各组物质在一定条件下反应,可以制得较纯净的氯乙烷的是( )
| A、乙烷与氯气混合 |
| B、乙烯与氯气混合 |
| C、乙烯与氯化氢气体混合 |
| D、乙烯通入浓盐酸中 |
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法错误的是( )
| X | Y | ||
| W | Z | ||
| T |
| A、X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B、物质W3X4中,每个原子最外层均达到8电子稳定结构 |
| C、X、Y和氢形成的化合物中可能既有离子键、又有共价键 |
| D、T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、25℃时,pH=12的1.0 L NaClO溶液中水电离出OH-的数目为0.01 NA |
| B、标准状况下,22.4 L甲醇中含有的氧原子数为1.0 NA |
| C、0.1 mol乙醇中含有0.6 NA个C-H共价键 |
| D、常温、常压下,3.5 g 35Cl2所含中子数为0.1 NA |

 B、
B、
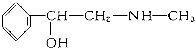 D、
D、 E、
E、