题目内容
13.17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol•L-1、c(N2O4)=0.0120mol•L-1.计算反应2NO2(g)?N2O4(g)的平衡常数K.(写出计算过程)分析 依据方程式,结合平衡等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积进行计算;
解答 解:17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol•L-1、c(N2O4)=0.0120mol•L-1.则反应2NO2(g)?N2O4(g)的平衡常数K=$\frac{c(N{\;}_{2}O{\;}_{4})}{{c}^{2}(NO{\;}_{2})}$=$\frac{0.0120}{0.0300{\;}^{2}}$=13.3L/mol;
答:平衡常数为13.3.
点评 本题考查化学平衡常数计算,难度不大,答题时注意根据平衡常数的定义进行计算.

练习册系列答案
相关题目
10.在温度相同、体积均为1L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下.已知:2SO2(g)+O2(g)?2SO3(g)△H=-98.3kJ•mol-1.
则:α1+α2=1,p=1.6mol,b+c=39.32kJ.
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | m mol SO2、n mol O2、p mol SO3 |
| c(SO3)/mol•L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
18.在一容积为2L的恒容密闭容器中加入0.2mol CO和0.4mol H2,发生如下反应:CO(g)+2H2(g)?CH3OH(g).实验测得,300℃下,CH3OH的物质的量随时间的变化如下表所示.
(1)20min内,v(CH3OH)=0.003mol/(L•min).
(2)该温度下反应的化学平衡常数数值为2.25×104 .
(3)H2的平衡转化率是90%.
(4)若实验测得500℃下,到达平衡时n(CH3OH)=0.160mol,则正反应是放热(填“放热”或“吸热”)反应.
| t/min | 10 | 20 | 30 | 40 | 50 | 60 |
| n(CH3OH)/mol | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
(2)该温度下反应的化学平衡常数数值为2.25×104 .
(3)H2的平衡转化率是90%.
(4)若实验测得500℃下,到达平衡时n(CH3OH)=0.160mol,则正反应是放热(填“放热”或“吸热”)反应.
5.下列关于钠与水反应的说法不正确的是( )
①将小块钠投入滴有石蕊试液的水中,反应后溶液变红
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④钠与氧气反应的产物为过氧化钠.
①将小块钠投入滴有石蕊试液的水中,反应后溶液变红
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④钠与氧气反应的产物为过氧化钠.
| A. | 只有①② | B. | 只有②③ | C. | 只有②③④ | D. | ①②③④ |
2.下列疾病与人体缺乏矿物质元素有关的是( )
| A. | 坏血病 | B. | 夜盲症 | C. | 骨质疏松 | D. | 糖尿病 |
3.对下列实验过程的评价,正确的是( )
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体一定含CO32- | |
| B. | 某无色溶液滴入酚酞试液显红色,该溶液呈碱性 | |
| C. | 某溶液中滴加BaCl2溶液生成不溶于稀硝酸的白色沉淀,该溶液可能含有SO42- | |
| D. | 验证烧碱溶液中是否含Cl-,先加稀盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl- |
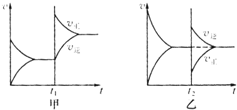 在一定条件下,有反应xA+yB?zC.
在一定条件下,有反应xA+yB?zC.