题目内容
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入l~2滴溴水,振荡后溶液呈黄色。
(1)提出问题: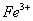 、
、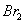 哪一个的氧化性更强?
哪一个的氧化性更强?
(2)猜想
①甲同学认为氧化性: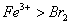 ,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性: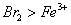 ,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(3)设计实验并验证
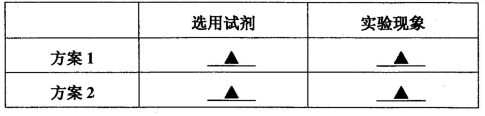
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。供选用的试剂:
| A.酚酞试液 | B.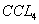 | C.无水酒精 | D.KSCN溶液 |
(4)应用与拓展
在足量的稀氯化亚铁溶液中加入l~2滴溴水,溶液呈黄色,所发生的离子反应方程式为: 。
(2)①Br2 ②Fe3+ (除方程式,每空1分)
(3)d 溶液呈红色 b CCl4层呈无色 (方案1与方案2答案可对换)
(4)2Fe2++Br2=2Fe3++2Br- (2分)
解析试题分析:(2)①如果氧化性: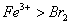 ,则上述实验现象不是发生化学反应所致,所以溶液呈黄色是含Br2所致。
,则上述实验现象不是发生化学反应所致,所以溶液呈黄色是含Br2所致。
②如果氧化性: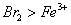 ,则单质溴就能把亚铁离子氧化生成铁离子,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致。
,则单质溴就能把亚铁离子氧化生成铁离子,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致。
(3)验证乙同学的观点,则就必须检验有铁离子生成,或者单质溴完全被反应而消耗。检验铁离子,可以用KSCN溶液。即答案选d,实验现象是溶液呈红色。由于单质溴易溶在有机溶剂中,所以可以选择四氯化碳,即答案选b,实验现象是CCl4层呈无色。
(4)该反应的离子方程式是2Fe2++Br2=2Fe3++2Br-。
考点:考查铁离子和单质溴氧化性强弱的实验探究
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生实验能力的培养和解题方法的指导与训练,有助于培养学生规范、严谨的实验设计能力。该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

 轻松暑假总复习系列答案
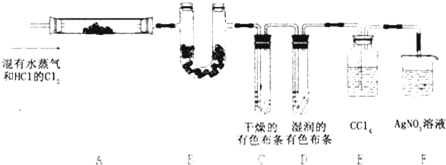
轻松暑假总复习系列答案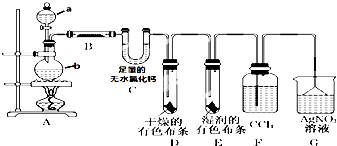 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称