题目内容
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略)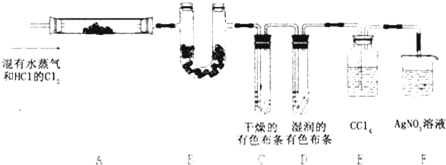
回答下列问题:
(1)装置A中盛放的试剂名称是
(2)装置C中和D中出现不同现象说明的问题是
(3)装置F中发生反应的离子方程式为
分析:(1)硫酸铜吸水生成蓝色硫酸铜晶体,检验是否含有水蒸气;
(2)干燥的氯气不能使有色物质褪色,氯气不具有漂白性;
(3)用AgNO3检验Cl-.
(2)干燥的氯气不能使有色物质褪色,氯气不具有漂白性;
(3)用AgNO3检验Cl-.
解答:解:验证Cl2中含有有水蒸气和HCl,装置A验证水,装置B吸收水,装置C和D验证Cl2的性质,装置E除Cl2,装置F验证HCl溶于水生成的Cl-.
(1)无水硫酸铜吸水能生成蓝色五水硫酸铜晶体,检验是否含有水蒸气;故答案为:无水硫酸铜;验证水蒸气;
(2)装置C中的现象可知:干燥氯气无漂白性,而装置D中氯气与水反应生成次氯酸,具有漂白作用;F装置用来检验HCl气体,因为Cl2溶于水可以生成Cl-,为了确保实验结论的可靠性,应排除氯气的干扰故,氯气易溶于四氯化碳,故可用四氯化碳来吸收氯气.
故答案为:氯气无漂白性,氯气溶于水生成的次氯酸有漂白性;防止氯气干扰氯化氢的检验;
(3)HCl溶于水生成H+和Cl-,可用AgNO3检验Cl-,若装置F有白色沉淀AgCl生成,则证明原气体中含有HCl,离子方程式为Ag++Cl-=AgCl↓.
故答案为:Ag++Cl-=AgCl↓.
(1)无水硫酸铜吸水能生成蓝色五水硫酸铜晶体,检验是否含有水蒸气;故答案为:无水硫酸铜;验证水蒸气;
(2)装置C中的现象可知:干燥氯气无漂白性,而装置D中氯气与水反应生成次氯酸,具有漂白作用;F装置用来检验HCl气体,因为Cl2溶于水可以生成Cl-,为了确保实验结论的可靠性,应排除氯气的干扰故,氯气易溶于四氯化碳,故可用四氯化碳来吸收氯气.
故答案为:氯气无漂白性,氯气溶于水生成的次氯酸有漂白性;防止氯气干扰氯化氢的检验;
(3)HCl溶于水生成H+和Cl-,可用AgNO3检验Cl-,若装置F有白色沉淀AgCl生成,则证明原气体中含有HCl,离子方程式为Ag++Cl-=AgCl↓.
故答案为:Ag++Cl-=AgCl↓.
点评:本题考查氯气的性质、氯离子检验等,难度不大,关键是清楚实验的目的与原理,注意用CCl4除尽Cl2.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
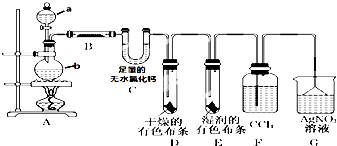 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称