题目内容
6.反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )①增加C的量
②保持体积不变,充入N2使体系压强增大
③将容器的体积缩小一半
④保持压强不变,充入N2使容器体积变大.
| A. | ①④ | B. | ①② | C. | ②③ | D. | ②④ |
分析 反应中固体参加,改变固体的量对反应速率没有影响,如气体的浓度不变,则反应速率不变,而浓度、压强、温度以及催化剂影响反应速率,以此解答该题.
解答 解:①C是固体,没有浓度可言,所以增加C的用量,不影响反应速率,故正确;
②保持体积不变,充入N2使体系压强增大,但参加反应气体的浓度不变,则反应速率不变,故正确;
③将容器的体积缩小一半,气体物质浓度增大,反应速率增大,故错误;
④保持压强不变,充入氮气使容器容积增大,参加反应的气体的分压减小,反应速率减小,故错误.
故选B.
点评 本题考查反应速率的影响因素,为考试高频考点,侧重考查学生的分析能力,难度不大,注意把握固体的特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.在一密闭容器中,反应 aA(气)?bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的65%,则下列说法正确的是( )
| A. | 平衡常数减小 | B. | 物质A的转化率增加了 | ||
| C. | 平衡向逆反应方向移动了 | D. | a>b |
11.下列反应中,不属于四大基本反应类型,但属于氧化还原反应的是( )
| A. | 2Na+2H2O=2 NaOH+H2↑ | B. | Cl2+H2O=HCl+HClO | ||
| C. | CaCO3=CaO+CO2↑ | D. | Ca(ClO)2+2HCl=CaCl2+2HClO |
15.如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是( )
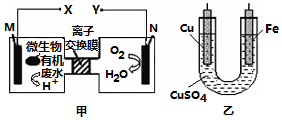

| A. | 质子透过离子交换膜由右向左移动 | |
| B. | 铜电极应与X相连接 | |
| C. | M电极反应式:(C6H10O5)n+7nH2O-24ne-═6nCO2↑+24n H+ | |
| D. | 当N电极消耗0.25 mol气体时,则铁电极增重16 g |
13.2A(g)+B(g)?3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
| A. | v(A)=0.7mol•L-1•min-1 | B. | v (B)=0.3mol•L-1•min-1 | ||
| C. | v (C)=0.9mol•L-1•min-1 | D. | v (D)=0.8mol•L-1•s-1 |

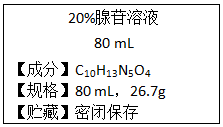 根据腺苷的相关信息,计算下列各题:
根据腺苷的相关信息,计算下列各题: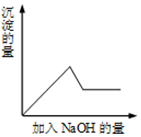 有一无色溶液,其中可能含有Fe3+、Cu2+、K+、Al3+、Mg2+、SO42-、Cl-等离子中的几种,为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如下:
有一无色溶液,其中可能含有Fe3+、Cu2+、K+、Al3+、Mg2+、SO42-、Cl-等离子中的几种,为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如下: